(54)发明名称
一种皮肤感染性压疮动物模型的构建方法及其应用
(57)摘要
本发明公开了一种皮肤感染性压疮动物模型的构建方法及其应用。本发明通过两个圆形磁铁夹小鼠背部皮肤的方法模型临床上压疮的发病过程,利用3‑氨基‑1 ,2 ,4‑三唑(ATZ)抑制过氧化氢酶,巯基琥珀酸(MSA)抑制谷胱甘肽过氧化物酶,提高损伤部位的过氧化氢,造成高水平氧化应激,并对伤口进行3M膜覆盖,延缓伤口愈合,促进伤口部位菌群的定植,自然形成多菌种感染伤口,降低小鼠模型的死亡率;最终形成了与临床病人压疮形成类型的模型伤口,可以用于研究皮肤压疮发生发展的分子机制、制备和/或筛选预防和/或治疗皮肤压疮的药物或优化手术治疗方案。
1 .一种皮肤感染性压疮动物模型的构建方法,包含以下步骤:
S1:选取实验小鼠,连续多天注射3‑氨基‑1 ,2 ,4‑三唑,在最后一天麻醉小鼠后再注射3‑氨基‑1 ,2 ,4‑三唑;
S2:将小鼠的背部正中两侧皮肤提起,成条状,两侧对称放置磁铁,使磁铁夹持条状皮肤,维持18~24h后去掉磁铁,在夹持的皮肤处涂抹或注射巯基琥珀酸重复2~4天;
S3:重复2~4天后将伤口部位使用医用3M透明膜覆盖14~28天,即获得压疮动物模型。
2 .根据权利要求1所述的构建方法,其特征在于,所述3‑氨基‑1 ,2 ,4‑三唑的剂量为2~5g/kg。
3 .根据权利要求1所述的构建方法,其特征在于,所述巯基琥珀酸的剂量为200~400mg/kg。
4 .根据权利要求1所述的构建方法,其特征在于,步骤S1中所述实验小鼠为7周~15月龄小鼠。
5 .根据权利要求1所述的构建方法,其特征在于,步骤S1中所述实验小鼠在开始造模前0 .5~1 .5个月进行开放式饲养;优选地,所述饲养条件包括:温度18‑22℃,湿度40%‑70%。
6 .根据权利要求1所述的构建方法,其特征在于,所述麻醉中采用的麻醉剂包括戊巴比妥钠,异氟烷,三溴乙醇,氯胺酮、甲苯噻嗪、乙酰丙嗪中的至少一种。
7 .根据权利要求1所述的构建方法,其特征在于,步骤S2中所述磁铁的面积为0 ..4~0 .6cm 2,厚度为2~4mm,磁力最高为2000~2400高斯。
8 .根据权利要求1所述的构建方法,其特征在于,所述磁铁包括圆形磁铁、方形磁铁、条形磁铁。
9 .根据权利要求1所述的构建方法,其特征在于,所述多天包括4~7天;优选地,步骤S2中去掉磁铁5‑30min后涂抹或注射巯基琥珀酸。
10 .权利要求1~9任一项所述的构建方法构建的动物模型在皮肤压疮发生发展的分子机制,或制备和/或筛选预防和/或治疗皮肤压疮的药物,或优化手术治疗方案中的应用。
一种皮肤感染性压疮动物模型的构建方法及其应用
技术领域
[0001]
本发明属于动物模型技术领域,具体涉及一种皮肤感染性压疮动物模型的构建方法及其应用。背景技术
[0002]
近年来,随着老龄化的加速到来,卧床的病人越来越多,压疮等感染性伤口发病率越来越高,严重影响人们健康。随着抗生素耐药性日益严重,感染性压疮的临床治疗效果不理想,尽管在了解感染性压疮如何发展方面投入了大量时间和精力,但基本问题仍未得到解答。其原因之一就是没有良好的动物模型。
[0003]
目前所用的皮肤感染性压疮动物模型具体制作如下:1、动物皮肤全层切除形成伤口后,向伤口部位定植已知的金葡菌、铜绿、大肠杆菌等形成感染。这种皮伤口感染菌群比较单一,和临床伤口存在多种菌群感染的现状不相符;2、动物皮肤全层切除形成伤口后,向伤口内移植肠道内容物(粪便)或污染的海水形成感染。这种皮肤伤口感染虽然可以形成多种菌群感染,但是其感染的菌群与皮肤伤口自然形成的菌群存在很大的差异;3、利用糖尿病动物模型,切除皮肤全层形成伤口后,腹腔注射和伤口涂抹促氧化应激药物各一次,自然形成伤口感染。这种皮肤伤口感染模型可以形成类似人类皮肤伤口自然感染的菌群,但是这种模型是切割形成的皮肤伤口,与压疮形成完全不同,而且小鼠的死亡率比较高。
[0004]
因此需要构建一种不需要切割,可以自然形成的皮肤感染性压疮动物模型。
发明内容
[0005]
本发明的目的在于提供一种新型的自然形成的皮肤感染性压疮动物模型。
[0006]
本发明所采取的技术方案是:
[0007]
一种皮肤感染性压疮动物模型的构建方法,包含以下步骤:
[0008]
S1:选取实验小鼠,连续多天注射3‑氨基‑1 ,2 ,4‑三唑,在最后一天麻醉小鼠后注射3‑氨基‑1 ,2 ,4‑三唑;
[0009]
S2:注射3‑氨基‑1 ,2 ,4‑三唑后将小鼠的背部正中两侧皮肤提起成条状,两侧对称放置磁铁,使磁铁夹持条状皮肤,维持8‑24h后去掉磁铁,在夹持的皮肤处涂或者注射抹巯基琥珀酸,重复2‑4天;
[0010]
S3:重复2~4天后将伤口部位使用医用3M透明膜覆盖14‑28天,即获得压疮动物模型。
[0011]
在本发明的一些实施方式中,步骤S1中所述实验小鼠为7周‑15月龄小鼠,可模拟从小鼠成年到中老年状态。
[0012]
在本发明的一些实施方式中,步骤S1中所述实验小鼠在开始造模前0 .5~1 .5个月进行开放式饲养。
[0013]
在本发明的一些实施方式中,所述饲养的条件为:饲养笼是开放式,温度18‑22,湿度40%‑70%。
[0014]
在本发明的一些实施方式中,所述小鼠包括C57BL/6小鼠、KM小鼠或ICR小鼠。
[0015]
在本发明的一些实施方式中,步骤S1中所述注射包括腹腔注射、皮下注射。
[0016]
在本发明的一些优选实施方式中,步骤S1中所述注射为腹腔注射,步骤S2中所述注射为皮下注射。
[0017]
在本发明的一些实施方式中,步骤S1中所述麻醉时使用的麻醉剂包括:戊巴比妥钠,异氟烷,三溴乙醇,氯胺酮(K)、甲苯噻嗪(X)、乙酰丙嗪(A)中的至少一种。
[0018]
在本发明的一些实施方式中,所述戊巴比妥钠的剂量为30‑90mg/kg。
[0019]
在本发明的一些实施方式中,所述异氟烷的剂量为3%~5%。
[0020]
在本发明的一些实施方式中,所述氯胺酮的剂量为60‑100mg/kg。
[0021]
在本发明的一些实施方式中,所述甲苯噻嗪的剂量为7‑20mg/kg。
[0022]
在本发明的一些实施方式中,所述乙酰丙嗪的剂量为0 .6‑3mg/kg。
[0023]
在本发明的一些实施方式中,所述麻醉剂包括氯胺酮、甲苯噻嗪、乙酰丙嗪。
[0024]
在本发明的一些实施方式中,所述麻醉剂的给药方式包括注射和吸入;优选为腹腔注射。
[0025]
在本发明的一些实施方式中,步骤S2中所述磁铁的面积为0 ..4~0 .6cm2,厚度2~4mm,磁力最高为2000~2400高斯。
[0026]
在本发明的一些实施方式中,所述磁铁优选为圆形磁铁、方形磁铁、条形磁铁。
[0027]
在本发明的一些实施方式中,所述磁铁直径为0 .7~1cm。
[0028]
在本发明的一些实施方式中,所述磁铁材质为钕铁硼强磁。
[0029]
在本发明的一些实施方式中,所述3‑氨基‑1 ,2 ,4‑三唑的剂量为2‑5g/kg。
[0030]
在本发明的一些实施方式中,步骤S2中去掉磁铁5‑30min后涂抹巯基琥珀。
[0031]
在本发明的一些实施方式中,所述巯基琥珀酸的剂量为200‑400mg/kg。
[0032]
本发明利用3‑氨基‑1 ,2 ,4‑三唑(ATZ)抑制过氧化氢酶,巯基琥珀酸(MSA)抑制谷胱甘肽过氧化物酶,以及3M膜,在伤口的不同时期处理,这样的处理方式,提高损伤部位的过氧化氢,造成高水平氧化应激,延迟伤口愈合促进伤口部位菌群的定植,自然形成多菌种感染伤口,同时降低了小鼠的死亡率。
[0033]
本发明的第二方面,提供由本发明第一方面所述的构建方法构建的动物模型在研究皮肤压疮发生发展的分子机制,或制备和/或筛选预防和/或治疗皮肤压疮的药物,或优化手术治疗方案中的应用。
[0034]
本发明的有益效果是:
[0035]
本发明提供了一种新型的自然形成的皮肤感染性压疮动物模型,选择7周~15个月龄的C57BL/6小鼠作为模型鼠,可模拟成年到中老年状态,并通过使用两个圆形磁铁夹小鼠背部皮肤的方法模型临床上压疮的发病过程,利用3‑氨基‑1 ,2 ,4‑三唑(ATZ)抑制过氧化氢酶,巯基琥珀酸(MSA)抑制谷胱甘肽过氧化物酶,提高损伤部位的过氧化氢,造成高水平氧化应激,并对伤口进行3M膜覆盖,延缓伤口愈合,促进伤口部位菌群的定植,自然形成多菌种感染伤口,降低小鼠模型的死亡率;最终形成了与临床病人压疮形成类型的模型伤口,可以用于研究皮肤压疮发生发展的分子机制、制备和/或筛选预防和/或治疗皮肤压疮的药物或优化手术治疗方案。
附图说明
[0036]
图1为造模后第3天,第7天,第14天和第28天伤口情况。
[0037]
图2为造模后第3天,第7天,第14天和第28天伤口皮肤HE染色。
[0038]
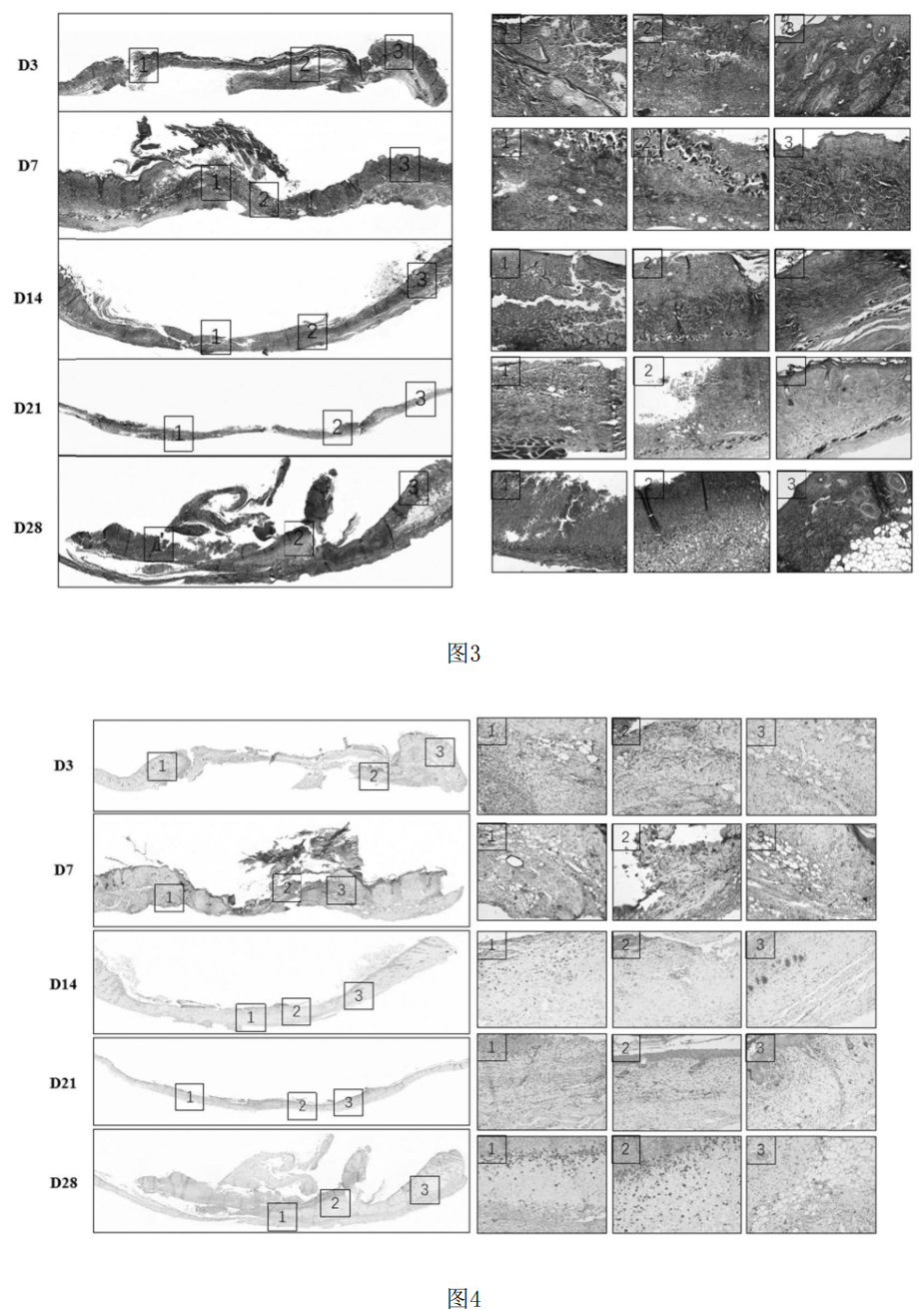
图3为造模后第3天,第7天,第14天和第28天伤口皮肤Masson染色。
[0039]
图4为造模后第3天,第7天,第14天和第28天伤口皮肤免疫组化检测iNOS标记M1型巨噬细胞。
[0040]
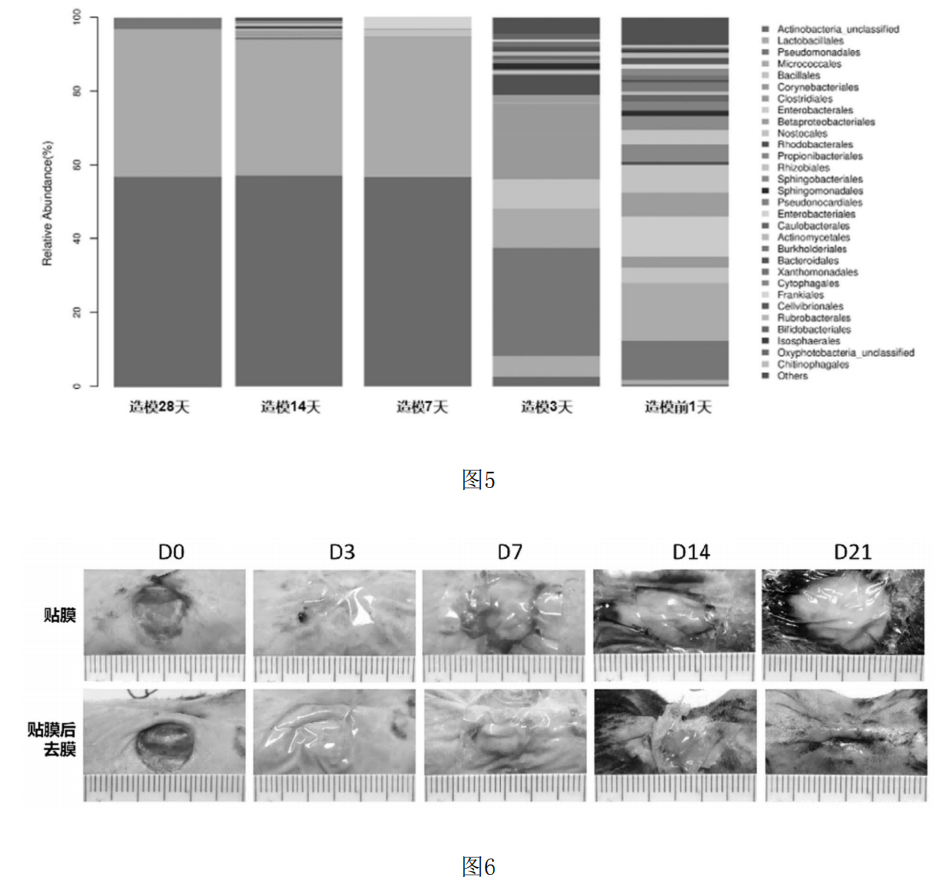
图5为造模后第3天,第7天,第14天和第28天伤口皮肤进行16SrDNA检测伤口部位菌群变化。
[0041]
图6为贴3M膜对伤口愈合的影响。
具体实施方式
[0042]
以下将结合实施例对本发明的构思及产生的技术效果进行清楚、完整地描述,以充分地理解本发明的目的、特征和效果。显然,所描述的实施例只是本发明的一部分实施例,而不是全部实施例,基于本发明的实施例,本领域的技术人员在不付出创造性劳动的前提下所获得的其他实施例,均属于本发明保护的范围。
[0043]
氨基‑1 ,2 ,4‑三唑,巯基琥珀酸,戊巴比妥钠,圆形磁铁(ATZ)购自于淘宝店铺:飞鸿磁业(购买网址为:https://m .tb .cn/h .UhotDep?tk=ObSUdcFkTXR);C57BL/6小鼠购自于南方医科大学实验动物中心;HE染色试剂盒,masson染色试剂盒,iNOS抗体购自于广州赛国生物科技有限公司;16SrDNA菌群检测杭州联川生物技术股份有限公司。
[0044]
实施例1
[0045]
1)选取15月龄小鼠,开始实验前1个月将这些小鼠开放式饲养,湿度为温度18‑22℃,湿度40%‑70%,便于小鼠皮肤形成成熟而复杂的皮肤微生物组。
[0046]
2)小鼠开放饲养1个月,腹腔注射3‑氨基‑1 ,2 ,4‑三唑(ATZ) (无菌PBS溶解,浓度200mg/ml,注射剂量是3g/kg,),左右腹部各一半体积,连续注射5天,第5天使用3%的戊巴比妥钠液腹腔注射(注射剂量30mg/kg)麻醉后,使用脱毛膏将小鼠背部毛发脱去,用无菌水清理皮肤,ATZ注射20分钟后,将沿背部正中线将背部皮肤提起,成条状,两边对称位置各放置一圆形磁铁(圆形磁铁直径为0 .8cm,厚度为3mm,磁力最高点约2200高斯),使磁铁夹持条状皮肤,12小时后,去掉圆形磁铁,10分钟后在夹持的皮肤处涂抹巯基琥珀酸(无菌PBS溶解,浓度200mg/ml,涂抹剂量为300mg/kg),每天一次,重复3天。
[0047]
3)3个重复后,伤口部位用医用3M透明膜覆盖,每天观察记录伤口情况,结果见图1,发现第1天溃疡部位组织坏死严重,伤口边缘发白,第3天溃疡部位开始出现黄色腐肉、有明显的渗出液和组织坏死,第7天溃疡部位腐肉组织和渗液增多,第14天溃疡部位依然有大量的腐肉组织,第21天溃疡部位仍覆盖有腐肉组织,第28天溃疡部位腐肉组织减少,伤口面积减小,至造模后第30天依然可以看到腐肉。
[0048]
4)造模后第3天,第7天,第14天、第21天和第28天取伤口部位皮肤进行HE染色,结果见图2,发现造模第3天皮肤部位由于缺血缺氧导致炎症细胞浸润,至第7天皮肤部位,表皮已经缺失,真皮处见大量坏死组织,炎症细胞大量浸润。第14天伤口部位坏死组织依然大量存在,炎症持续存在。第28天,伤口部位坏死组织和炎症依然存在,部位仍未愈合,有大量炎症细胞浸润,其损伤过程和组织形态与临床压疮表型十分吻合。
[0049]
5)造模后第3天,第7天,第14天、第21天和第28天取伤口部位皮肤进行masson染色,结果见图3,发现造模第3天开始伤口部位大量坏死组织,纤维破坏严重,至28天伤口部位仍有大量坏死组织。
[0050]
6)造模后第3天,第7天,第14天、第21天和第28天取伤口部位皮肤,免疫组化检测伤口部位M1巨噬细胞,结果见图4,结果发现,伤口部位大量的M1型巨噬细胞。
[0051]
7)造模前1天,造模后第3天,第7天,第14天和第28天取伤口部位皮肤进行16SrDNA检测伤口部位菌群变化,结果见图5,结果发现与造模前1天伤口部位的菌群分布相比,伤口部位的菌群由正常的菌群多样性,变成单一致病菌占据主要。
[0052]
8)实验用小鼠9只,成功9只,没有出现死亡小鼠,建模成功率100%。
[0053]
实施例2
[0054]
关于3M膜,3M透明敷贴在临床上常应用于各类留置针、导管的固定等,是一种新型的卫生材料,有防水、透气,低过敏性,有效隔绝水、细菌及灰尘,对皮肤刺激性小。本发明发现,对伤口进行3M膜覆盖,延缓伤口愈合,可以看到贴膜后伤口一直未愈合,但是当在第14天去除3M膜,伤口很快愈合(图6)。
[0055]
上述具体实施方式对本发明作了详细说明,但是本发明不限于上述实施例,在所属技术领域普通技术人员所具备的知识范围内,还可以在不脱离本发明宗旨的前提下作出各种变化。此外,在不冲突的情况下,本发明的实施例及实施例中的特征可以相互组合。