下肢动脉粥样硬化性疾病(LEAD)是全身动脉硬化在肢体局部的表现,是老年人常见的一种肢体慢性缺血性疾病,已被 NCEP ATP Ⅲ[1]列为冠心病的等危症。临床上,LEAD 涵盖了一组临床特点、危险层次及预后极不均一的疾病群体,目前人们已对老年 LEAD 及其相关危险因素开展研究,但不同年龄层次、不同严重程度 LEAD 与各危险因素之间的相关性及特点尚不完全清楚。本文针对老年(特别是高龄老年人)这一特殊群体,通过彩色多普勒超声检测患者下肢动脉粥样硬化情况,比较各年龄层次、不同严重程度 LEAD 各危险因素的特点,分析其相关性,探讨高危因素,为其防治提供依据。
1 资料与方法
对 象 : 连 续 选 取 2013-05 至 2014-11 于我院老年病科行下肢动脉彩色多普勒超声检查的住院患者共 700 例。根据年龄分为青中年组(42~59 岁 )83 例, 平 均(54.99±4.18) 岁;老年 组(60~79 岁 )377 例, 平 均(70.01±5.87)岁;高 龄 老 年 组(80~100 岁 )240 例, 平 均(84.06±3.51)岁。根据动脉硬化严重程度,其中正常患者 112 例,平均(62.51±7.96)岁,轻度硬化 81 例,平均(68.14±8.17)岁,中度硬化 466例,平均(75.65±9.49)岁,重度硬化 41 例,平均(81.88±7.12)岁。排除标准[2]:(1)急性动脉栓塞;(2)血栓闭塞性脉管炎;(3)多发性大动脉炎;(4)结节性多动脉炎;(5)特发性动脉血栓形成;(6)需与可引起假性间歇性跛行的其他疾病,包括神经根压迫、椎管狭窄、有症状的贝克氏囊肿、慢性肌筋膜综合征、神经性疼痛、髋关节炎等鉴别。
方法 : (1)临床资料:对所有研究对象详细询问病史,记录年龄、性别、吸烟史、高血压病史、糖尿病史。检测血清甘油三酯(TG)、总胆固醇(TC)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)、血清肌酐(Cr)、尿酸(UA)、超敏 C
反应蛋白(hs-CRP)、糖化血红蛋白(HbA1c)、血浆纤维蛋白原(Fib)、空腹血糖(FBG)、早餐后 2 小时血糖(2hPBG);收集研究对象的血压、身高(cm)、体重(kg)、踝肱指数(ABI)值,计算体重指数(BMI)= 体 重 / 身 高2(kg/m2)。(2) 诊 断 标 准:采 用 GEvivid7 型彩色多普勒超声检测仪,线阵式探头频率10 MHz,受检者充分暴露下肢,取仰卧或俯卧位,检测股总动脉、股深动脉、股浅动脉、腘动脉、胫前动脉、胫后动脉。动脉内中膜厚度(IMT)测量和增厚标准 : 上述任一动脉横断面 IMT 最厚处测量,正常 IMT < 1.0 mm[3,4],IMT ≥ 1.0 mm 定义为内膜增厚。斑块定义及测量[4]: 下肢动脉横断面 IMT 最厚处测量,局限性 IMT 增厚凸入动脉管腔≥ 0.5 mm,或较周围 IMT 增加超过 50%,或 IMT > 1.5 mm 定义为斑块。根据下肢动脉彩色超声结果进行严重程度评分[5],标准:①动脉内膜厚度:正常(< 1 mm)0分,轻度增厚(1.0~1.2 mm)1 分,中重度增厚(> 1.2mm)2 分。②硬化程度:正常 0 分,轻度硬化(内膜不厚但回声强,无斑块)1 分,中重度硬化(轻度伴斑块或狭窄)计 2 分。③斑块:正常 0 分,单发 1 分,多发 2 分,弥漫 3 分。④狭窄:正常 0 分,轻度狭窄(狭窄 30% ~50%)1 分,中重度狭窄(狭窄 50%~75%)2 分,闭塞(> 75% ~ 无血流 )3 分。用总分评定病变严重性:① 0 分为正常。② <10 分为轻度。③ 10~19 分为中度。④≥ 20 分为重度。
统计学方法 : 应用 SPSS 19.0 统计软件,计量资料用 ±s 表示,计数资料以例数或百分比(%)表示,两组间均数比较采用 t 检验,组间率的比较采用 χ2检验,多组间均数比较采用单因素方差分析。相关性采用 Logistic 回归分析。P<0.05 为差异有统计学意义。
2 结果
不同年龄组间临床基线资料比较(表 1): 与青中年组比较,老年组人群高血压患病率、Fib、Cr、hs-CRP 较高,DBP、TC、ABI 较低;差异有统计学意义(P 均 <0.05~0.01)。与青中年组比较,高龄老年组高血压患病率、SBP、Fib、Cr、UA、hs-CRP较 高,BMI、DBP、TG、TC、LDL-C、ABI 较 低,差异有统计学意义(P 均 <0.05~0.01)。与老年组比较,高龄老年组高血压患病率、Fib、Cr、UA、hs-CRP 较高,BMI、DBP、TG、TC、ABI 较低,差异有统计学意义(P 均 <0.05~0.01)。
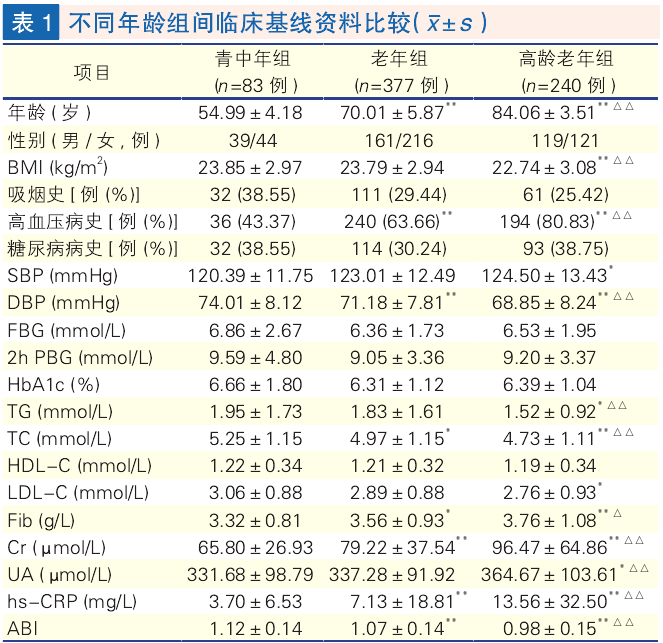
注: BMI:体重指数 ; SBP:收缩压 ; DBP:舒张压 ; FBG:空腹血糖 ;2 h PBG:早餐后 2 h 血糖 ; HbA1c:糖化血红蛋白 ; TG:甘油三酯 ; TC:胆固醇 ; HDL-C:高密度脂蛋白胆固醇 ; LDL-C:低密度脂蛋白胆固醇 ; Fib:血浆纤维蛋白原 ; Cr:血清肌酐 ; UA:尿酸 ; hs-CRP:超敏 C 反应蛋白 ;ABI:踝肱指数。与青中年组比较*P<0.05**P<0.01;与老年组比较△P<0.05△△P<0.01。1 mmHg=0.133 kPa
不同严重程度下肢动脉粥样硬化患者基线资料比较(表 2): 随动脉硬化严重程度加重,年龄呈明显上升趋势,差异有统计学意义(P 均 <0.01)。与正常患者比较,轻度硬化患者 Cr、UA 较高,ABI较低,差异有统计学意义(P 均 <0.05~0.01);与正常患者相比,中度硬化患者具有较高的男性百分比、吸烟率、高血压及糖尿病患病率,SBP、FBG、2 h PBG、Fib、Cr、UA、hs-CRP 亦 较 高,BMI、TC、HDL-C、ABI 较低,差异有统计学意义(P 均<0.05~0.01);与正常患者相比,重度硬化患者具有更高的男性百分比、吸烟率、高血压患病率,SBP、2 h PBG、HbA1c、Fib、Cr、UA、hs-CRP 均 较 高,而 TC、HDL-C、ABI 较低,差异有统计学意义(P均 <0.05~0.01)。与轻度硬化患者比较,中度硬化患者男性百分比、高血压患病率、SBP、FBG、Cr、UA 较高,HDL-C、ABI 较低,差异有统计学意义(P均 <0.05~0.01);与轻度硬化患者相比,重度硬化患者男性百分比、吸烟率、高血压患病率、SBP、Fib、Cr、UA、hs-CRP 更高,ABI 明显偏低,差异有统计学意义(P 均 <0.05~0.01);与中度硬化患者比较,重度硬化患者高血压患病率、Fib、UA 较高,ABI 较低,差异有统计学意义(P 均 <0.01)。

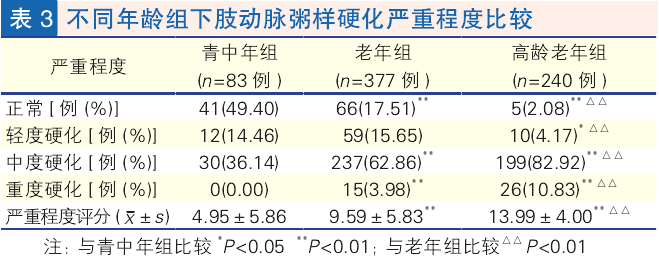
不同年龄组下肢动脉粥样硬化严重程度比较(表 3): 年龄越大,严重程度评分越高(P 均<0.01)。与青中年组相比,老年组、高龄老年组中、重度硬化病变率明显较高;高龄老年组中、重度硬化病变率较老年组高(P 均 <0.01)。
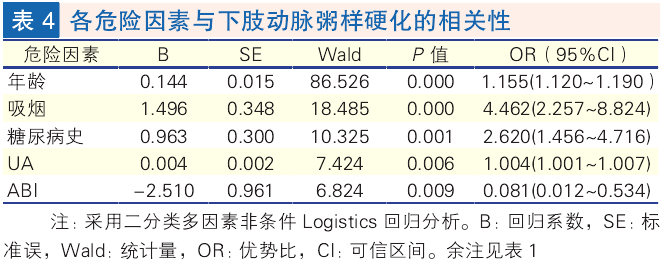
下肢动脉粥样硬化危险因素的多因素分析(表 4): 以有无下肢动脉粥样硬化为因变量,各危险因素为自变量进行多因素非条件 Logistics 回归分析,年龄、吸烟、糖尿病史、UA、ABI是下肢动脉粥样硬化的独立危险因素(P 均 <0.01),其中 ABI 与其呈负相关。
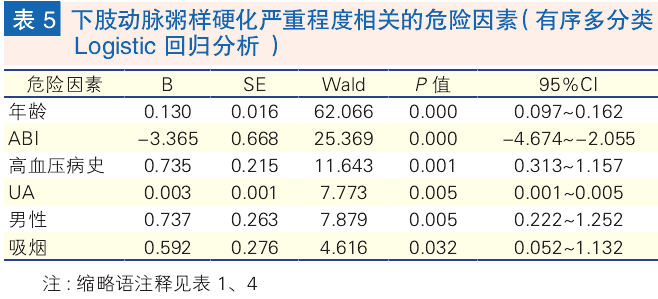
与下肢动脉粥样硬化严重程度相关的危险因素(表 5):以下肢动脉粥样硬化严重程度为因变量,以各危险因素为自变量进行有序多分类 Logistic 回归分析,年龄、男性、吸烟、ABI、UA、高血压病史与动脉硬化严重程度相关(P 均 <0.05)。
3 讨论
本研究通过彩色多普勒超声检测下肢动脉内膜厚度、硬化程度、斑块及狭窄,诊断 LEAD 并按其严重程度分组,着重对高龄老年及不同程度动脉硬化人群进行分析研究,探讨其特点及危险因素分布。
本研究显示,年龄越大,动脉硬化严重程度评分越高;老年、高龄老年组中、重度硬化病变率明显较高;多因素回归分析显示增龄是下肢动脉粥样硬化的独立危险因素,且与其严重程度密切相关。伴随增龄,血管弹性减退,内皮细胞逐渐凋亡、内皮功能下降;合并心血管及代谢性疾病渐增多,协同促进动脉粥样硬化的发生与发展。因此,增龄是动脉粥样硬化不可控制的危险因素。
本研究发现,中、重度下肢动脉硬化患者男性百分比显著高于正常及轻度硬化患者,有序多分类回归分析亦显示男性与动脉硬化严重程度呈正相关。Framingham 研究显示,男性下肢动脉硬化闭塞症患病率相对高于同龄女性。其致动脉粥样硬化可能与男性睾酮水平有关,老年睾酮水平降低,低睾酮水平可降低血管内皮功能而促发动脉粥样硬化[6]。研究表明血睾酮水平与 TC、TG、LDL-C、脂蛋白(a)呈负相关[7],均可促进动脉粥样硬化的形成。
本研究显示,中、重度下肢动脉硬化患者吸烟率明显较高,多因素 Logistic 回归分析示吸烟与下肢动脉粥样硬化及其严重程度密切相关。香烟中的有害物质使血管内皮功能受损,合成释放一氧化氮减少,内皮依赖性血管舒张功能受损,同时可促进血小板聚集、黏附和纤维蛋白原沉积[8],诱发动脉粥样硬化。亦有研究提出吸烟可促进 TC 在动脉内膜下沉积,同时降低 HDL-C 水平[9],协同促进动脉粥样硬化的形成与发展。Framingham 研究强调,吸烟者外周动脉粥样硬化性疾病的发生率是非吸烟者的 2~4 倍。
高血压是冠心病、脑卒中、动脉粥样硬化的主要危险因素。本研究中,高血压患病率随增龄上升,合并下肢动脉硬化严重程度加剧。老年、高龄老年组高血压患病率较青中年组增加,高龄老年组高血压患病率亦较老年组增加;中、重度下肢动脉硬化患者高血压患病率较正常及轻度硬化者高,重度硬化患者高血压患病率亦较中度硬化者高,且以收缩压升高为主。有序多分类 Logistic 回归分析显示高血压与动脉粥样硬化严重程度密切相关。Framingham研究报道在男性高血压患者中外周动脉粥样硬化疾病患病率为非高血压患者的 2.5 倍,女性为 3.9 倍。
本研究发现,中度下肢动脉硬化患者糖尿病患病率、FBG、2h PBG 较正常患者高,重度硬化患者 2hPBG、Hb A1c 较正常患者高,提示血糖控制不良会促进下肢动脉粥样硬化的发生。多因素 Logistic 回归分析亦显示糖尿病是下肢动脉粥样硬化的独立危险因素。糖尿病引起动脉硬化是一个长期、慢性的过程,其机制可能是:血糖升高,氧化应激性增加,大量自由基产生致血管内皮细胞功能障碍,强化白细胞与内皮细胞间的相互作用,低密度脂蛋白氧化和糖基化及糖基化终产物沉积引起的一系列连锁反应[10]。糖尿病患者下肢血管疾病患病率是非糖尿病患者的 20 倍[11]。
本研究中,随增龄及动脉硬化程度加重,TG、TC、LDL-C 呈降低趋势,与既往高血脂引起动脉粥样硬化的结论不符,其原因可能与绝大多数老年人既往合并高脂血症或动脉硬化性疾病长期服用调脂药物有关。研究认为高血脂可引起内膜增厚,内弹力板部分断裂,内膜下脂质和胶原纤维沉积、泡沫细胞和炎性细胞浸润、平滑肌细胞迁移、增生,这是动脉粥样硬化的病理表现,也是血管重塑的病理学基础[12]。本研究 HDL-C 随增龄、动脉硬化程度加重而渐降低,中、重度动脉硬化患者明显低于正常患者。HDL-C 将胆固醇逆向运输至肝脏降解,降低胆固醇水平,从而抵抗动脉粥样硬化,HDL-C 降低致血管内皮细胞中胆固醇积聚,加速动脉粥样硬化的形成与发展。
ABI 公认为下肢血管疾病的早期筛查、诊断方法,本研究进一步验证了其可靠性及与彩色超声诊断的一致性。本研究发现,随增龄、下肢动脉硬化严重程度加重,ABI 明显降低,Logistic 回归分析亦提示其与下肢动脉粥样硬化呈负相关。此外,本研究可见随增龄、下肢动脉硬化严重程度加重,UA、Cr、Fib、hs-CRP 渐升高,多因素Logistic 回归分析显示 UA 是下肢动脉粥样硬化的独立危险因素,且与其严重程度相关。上述因素均是动脉粥样硬化性疾病常见危险因子,通过多种途径参与其发生、发展。
动脉粥样硬化被视为一种与衰老相关的疾病,本研究特别关注高龄老年人这一特殊群体,表 2 中可见高龄老年组高血压患病率明显升高,呈 SBP 升高、DBP 降低,符合老年人以收缩压升高为主,脉压差增大的特点;UA、Cr、Fib、hs-CRP 亦显著升高,如上所述,它们协同促进下肢动脉粥样硬化的发生与发展。高龄老年人下肢动脉粥样硬化除上述传统危险因素外,与细胞生理性老化亦相关,动脉粥样硬化斑块作为细胞衰老的证据显示其特征为细胞增殖减少,不可逆的细胞生长停滞和凋亡,DNA 损伤升高,端粒缩短和功能障碍,细胞衰老促进动脉粥样硬化的进展[13]。炎症反应学说作为动脉粥样硬化的发病机理之一,衰老与动脉壁炎症活动的增强亦有关,伴随增龄血管黏附分子 1(VCAM-1)水平显著升高,VCAM-1 表达的内皮细胞介导单核细胞粘附和聚集于内皮边缘,参与动脉粥样硬化的形成[14]。平滑肌细胞(VSMCs)增殖是动脉粥样硬化的一个关键性事件,老化使 VSMCs 从中膜迁移积聚到血管内膜,致动脉内膜增厚诱发动脉粥样硬化;VSMCs 属性改变是动脉壁病理学的重要事件,它导致随老化引起的血管重塑和功能下降,促进动脉粥样硬化的进展[15]。动物实验表明,血液中来源于骨髓的内皮祖细胞随年龄增长而渐耗竭,致内皮祖细胞修复内皮损伤的能力下降,更易形成动脉粥样斑块,促发动脉粥样硬化性疾病[16]。综上,高龄老年人群受多重传统危险因素和衰老引起机体本身的病理生理学改变的影响,致下肢动脉粥样硬化加重。
本研究的局限性:因大多受试者合并高血压、糖尿病、冠心病、高脂血症等慢性疾病,在入院前及住院期间均按相应适应症不同程度地接受调脂药物、血管扩张药物、抗血小板药物、降糖药物等治疗,所以上述药物对动脉粥样硬化的影响及相关性难以衡量。
综上所述,本研究发现老年人下肢动脉粥样硬化与多种心血管危险因素相关。增龄、吸烟、糖尿病史、UA、ABI 是下肢动脉粥样硬化的独立危险因素,且高龄、男性、吸烟、UA、ABI、高血压病史与其严重程度相关。控制上述危险因素对延缓乃至逆转下肢动脉硬化的发展尤为重要,将降低其致残率、致死率,进而提高老年下肢动脉粥样硬化患者生活质量与期望寿命。
来源:中国循环杂志 2015 年 11 月 第 30 卷 第 11 期(总第 209 期)


