其实为了做到这「一天之计在于晨」的精神满满,我们的身体悄无声息、未雨绸缪地干了很多活,在我们睡得正酣的凌晨就已开始早早做着一系列的工作,来蓄满这清晨的「能量」。
每一个健康人,在「指挥中枢」下丘脑的调控下,下丘脑-垂体-靶腺以其特有的工作模式传递信息为清晨「储能充电」。
在凌晨 1:00-4:30 生长激素分泌达到高峰,4-6 点皮质醇、肾上腺素和去甲肾上腺素分泌增加,5:30 以后肝葡萄糖生成增加。
身体「蓄力充电」的同时会随之带来血糖的升高,这时用来平衡血糖的胰岛素分泌同时也会增加,外周葡萄糖利用同时增加,因此健康人在凌晨至清晨时分的血糖维持稳定,升高不明显 [1],因此非糖尿病人群中不存在黎明现象。
糖尿病患者与健康人类似,生长激素、皮质醇、肾上腺素、去甲肾上腺素的分泌在凌晨增加。
但是肝葡萄糖生成增加过早开始出现,同时并没有相对应出现平衡血糖的胰岛素分泌节律的变化,加之胰岛素抵抗的存在,肝脏和外周胰岛素敏感性降低,外周葡萄糖利用减少,血浆葡萄糖浓度升高,出现了黎明现象(dawn phenomenon)[2]。
Monnier 等研究认为黎明现象是 2 型糖尿病自然病程中糖调节受损最早期的表现形式 [3]。
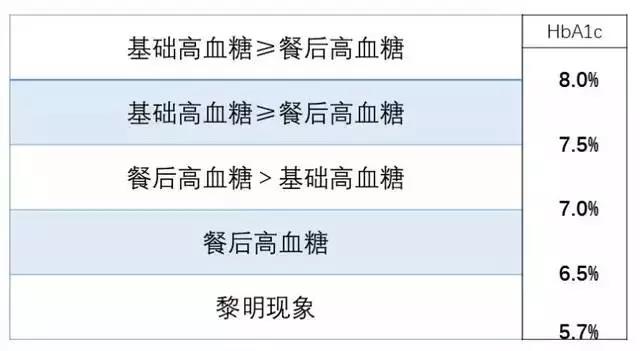
表:糖尿病自然病程模式图 [4]
糖尿病并发症或止于它
黎明现象最早在 1981 年由 Schmidt 提出。众多关于黎明现象发生率的报道差异较大,有报道认为 55% 的 1 型糖尿病患者和 54% 的 2 型糖尿病患者存在黎明现象。
目前认为清晨至早餐前血糖升高属于黎明现象,早餐后血糖的异常升高属于延伸的黎明现象(extented dawn phenomenon)。黎明现象的病理机制目前认为在胰岛素β细胞功能衰退、胰岛素抵抗的基础上,凌晨内源性升糖量增加,以生长激素为主的胰岛素拮抗性激素的升高进一步加重了胰岛素抵抗,最终出现黎明现象。
Monnier 等对黎明现象的定量化研究,显示黎明现象可以使 HbA1c 增加 0.4% 左右,而 HbA1c 每下降 1% 可减少 40% 的大血管并发症,减少 37% 的微血管并发症。对通过比较 HbA1c 范围在 6.5%-6.9% 和 7.0%-7.9% 的患者,其早间血糖(早餐前至早餐后 3 h)均值有明显差别(7.5 mmol/L 比 9.3 mmol/L,P = 0.0003),提示对于 HbA1c<8.0% 的患者,进一步的降低血糖可能需要有效控制黎明现象以辅助达标(<7.0%)[5]。
因此,控制黎明现象对血糖达标、减少并发症的潜在影响不容小觑。
口服降糖药不达标,起始胰岛素或也因为它
有研究提示,无论单一口服降糖药物治疗或是联合口服降糖药物治疗,或不能充分控制黎明现象。
因此《中国 2 型糖尿病防治指南(2013 版)》提出,经过较大剂量多种口服药物联合治疗后 HbA1c 仍 ≥ 7.0% 时,即要考虑启动胰岛素治疗。
由此,也可以看出黎明现象的重要性,针对性的治疗黎明现象,降低晨间血糖,可能是控制全天血糖的关键,是长期控糖、积极防治并发症的突破点。
黎明现象判断标准
黎明现象的判定主要是基于夜间血糖和早餐前血糖水平之间的差异,即计算夜间血糖最低值和早餐前血糖值之间的绝对差值。既往通过每半小时抽取静脉血计算血糖差值,目前可以通过动态血糖监测判定黎明现象,现认为绝对差值> 1.11 mmol/ L(20 mg/ dL) 具有最佳的判定意义。
动态血糖监测的受设备及费用的影响,使其应用受到一定限制。Monnier 等提出通过更简便易行、更易在基层推行的判定方法:
通过自我血糖监测的方法,监测三次正餐前血糖的办法来预测是否存在黎明现象。血糖监测获取早餐前、午餐前、晚餐前的血糖数值,计算早餐前血糖与午餐前、晚餐前平均血糖的绝对差值作为判断黎明现象的标准。以绝对差值>0.56 mmol/L(10 mg/dL)作为标准的敏感度 71%、特异度 68%[6]。
这种方法对于患者及医生来说都较为简便可行,但有待进一步验证。
黎明现象应对策略
当 HbA1c< 7. 0% 时, 黎明现象仍相对可控, 一般采取饮食疗法或联合降低空腹血糖为主的口服药物治疗。如睡前口服二甲双胍,通过减少内源性葡萄糖产生, 增强基础状态下糖酵解, 减轻胰岛素抵抗控制黎明现象。
当 HbA1c>7. 0% 时,口服降糖药由于对黎明现象控制有限,且磺脲类降糖药增加夜间低血糖的问题,胰岛素治疗应是首先考虑的方案。基础胰岛素或持续皮下输注胰岛素的应用均有利于控制黎明现象和长期血糖的稳定达标。
目前证据也支持 HbA1c< 7. 0% 的患者, 采用基础胰岛素治疗, 也可以降低夜间高血糖和黎明现象, 从中获益。
其他控制黎明现象的药物主要有赛庚啶, 通过较强的抗组胺与抗 5-羟色胺作用, 抑制垂体前叶分泌生长激素及促肾上腺皮质激素。近年来, 一些新兴的药物,如 FGF-21 类似物、缓释的新型 GH 抑制剂培维索孟等,也为黎明现象的治疗提供了新的治疗策略。
文 | 田建卿,新疆军区总医院内分泌科主任、医学博士
责任编辑 | 小平筒子
参考文献:
[1]Boden G, Ruiz J, Urbain JL, et al. Evidence for circadian rhythm of insulin secretion[J]. Am J Physiol, 1996,271(2 Pt 1):E246-252.
[2]Campbell PJ, Bolli GB, Cryer PE, et al. Sequence of events during development of the dawn phenomenon in insulindependent diabetes mellitus[J]. Metabolism, 1985, 34(12):1100-1104.
[3]Monnier L, Colette C, Dejager S, et al. Residual dysglycemia when at target HbA(1c) of 7% (53 mmol/mol) in persons with type 2 diabetes[J]. Diabetes Res Clin Pract,2014 ,104(3):370-375.
[4]Monnier L, Colette C, Dejager S, et al. "Mild dysglycemia" in type 2 diabetes: to be neglected or not[J] Diabetes Complications. 2015,29(3):451-458.
[5]Monnier L, Colette C, Dunseath GJ, et al. The loss of postprandial glycemic control precedes stepwise deterioration of fasting with worsening diabetes[J]. Diabetes Care, 2007, 30(2): 263-269.
[6]Monnier L, Colette C, Dunseath GJ, et al. The dawn phenomenon in type 2 diabetes: how to assess it in clinical practice[J] Diabetes Metab. 2015,41(2):132-137.


