皮肤承担着多种重要功能,包括屏障、体温调节和免疫防御等。 其中皮肤屏障对内能有效避免体内水分和营养物质的流失,对外能防止外界物理、化学、生物及紫外线等因素对皮肤的损害[1] 。
从细胞分化及组织学结构分析,表皮的物理性屏障不仅局限于角质层( stratum corneum,SC),还累及颗粒层(stratum granulosum,SG)、棘层(stratum spinosum,SS)及基底层(stratum basale,SB)的结构功能;从生化组成及功能作用分析,表皮的物理屏障与表皮脂质的组成、表皮各层基因表达及其他代谢产物的相互作用息息相关[2] 。 这些成分的任何异常都有可能影响表皮屏障功能,诱发或加重皮肤病的发生及反复。
1983 年,美国加州大学 Peter M. Elias 教授提出角质层“砖墙结构”[3]。 2002 年,日本京都大学 Mikio Furuse教授首次证明紧密连接( tight junction,TJ)蛋白参与维持皮肤屏障功能[4] 。 TJ 蛋白主要分布在颗粒层、棘层及基底层[5] 。 尽管研究表明皮肤屏障受损发生在表皮不同层次,但缺乏对表皮不同层次受损机制及精准干预手段的系统探讨。 本文从表皮组织结构及生化组成对常见皮肤疾病及皮肤问题表皮屏障分层受损机制进行探讨,提出“表皮屏障受损及分层修复”新理念,为皮肤疾病及皮肤问题的精准干预提供新思路。
1表皮屏障的主要结构与功能
1. 1 角质层“砖墙结构” 角质层的屏障功能主要由角质细胞和细胞间脂质构成,两者共同形成了皮肤屏障特有的“砖墙结构”。 角质形成细胞从基底层起始,逐步迁移至表层,在此过程中经历了棘层和颗粒层的脱核和扁平化,最终形成角质细胞。 角质细胞像“砖块”一样在角质层有序排列[3] 。 角质细胞的细胞膜间存在角质细胞角化包膜(cornified envelope,CE),主要由兜甲蛋白( loricrin,LOR)、内披蛋白( involucrin,INV)、丝聚蛋白(filaggrin,FLG)以及晚期角化包膜蛋白( late cornified envelope proteins,LCEs)等多种蛋白质交联而成[6] 。
CE 与细胞间脂质相互交织,共同形成一道强大的防护屏障,可增强表皮渗透性屏障的稳定性。 细胞间脂质类似砌墙使用的“灰浆”,主要由 50%神经酰胺(ceramide,Cer)、25%胆固醇(cholesterol,CHOL)与 15%游离脂肪酸(free fatty acid,FFA) 组成[7] 。 正常的细胞间脂质含量和比例对皮肤屏障功能的维持至关重要[8] 。 当蛋白表达异常、灰浆成分减少或比例失衡,角质层“砖墙”结构稳定性降低,将诱发或加重皮肤病的发生及反复。
1. 2 紧密连接 TJ 是角质形成细胞间的重要连接结构,由跨膜蛋白和胞内蛋白组成。 这些跨膜蛋白在细胞外通过相互作用,形成类似“拉链”的紧密结构,连接相邻细胞,并有效封闭细胞间隙。 具体而言,TJ 像闸门一样将颗粒层、棘层和基底层的角质形成细胞紧密连接,阻止细胞间的物质渗透[9] 。 TJ 被认为是调节表皮屏障功能的“关键控制因子”[10]。 当 TJ 蛋白表达异常时,表皮屏障受损,将诱发多种皮肤疾病及皮肤问题发生。
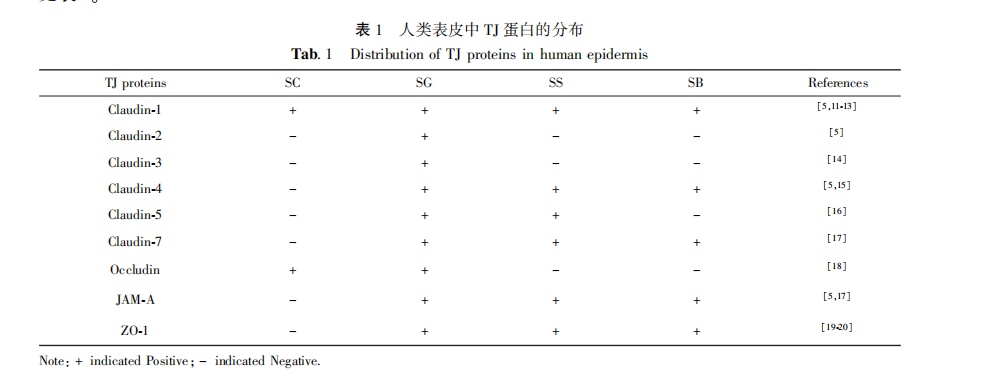
跨膜蛋白包括 Claudins、Occludin、连接素黏附分子(junctional adhesion molecule,JAM)家族等,其细胞外环部分可互相融合,封闭细胞间隙;胞浆蛋白包括 ZO⁃1、ZO⁃2 和 ZO⁃3 等,可连接跨膜蛋白与细胞骨架蛋白。其中,Claudins 是组成 TJ 结构最重要的蛋白家族,其家族成员有 Claudin⁃1 ~ Claudin⁃27,这些蛋白分别由基因 CLDN1 ~ CLDN27 编码。 Claudins 在表皮中的分布模式呈现出一定的多样性。 人类表皮中 TJ 蛋白的分布见表 1。
2 皮肤疾病及皮肤问题表皮不同层次受损机制
2. 1 特应性皮炎 特应性皮炎( atopic dermatitis,AD)的皮肤屏障功能受损与角质层蛋白、脂质组成相关。Haftek 等[11]研究表明,FLG 缺乏会导致角质层含水量下降,经表皮失水率( trans epidermal water loss,TEWL)增加,从而削弱屏障功能。 Yoshida 等[19]发现,AD 患者角质层中 Cer 和长链 FFA 减少,短链脂质比例增加,导致脂质层排列紊乱、密度降低,进一步加剧 TEWL 升高和微生物入侵。
Asad 等[21]研究表明,AD 患者表皮(皮损区和非皮损区)的 Claudin⁃1 水平均显著减少,从而破坏 TJ 结构功能,导致皮肤屏障受损,揭示 Claudin⁃1 在 AD 发生中的关键作用。 Claudin⁃1 的减少累及表皮全层,提示皮肤屏障修复应兼顾表皮多个层次。 Ryu 等[22]研究发现,IL⁃33 通过 ERK/ STAT3 信号通路导致角质形成细胞中 Claudin⁃1 表达下调,进而引起皮肤屏障功能受损。 Bergmann 等[23] 进一步研究发现,Claudin⁃1 降低会诱导角质形成细胞中 IL⁃1β 表达,促进 AD 炎症细胞浸润,加剧 AD 炎症反应。2. 2 痤疮 痤疮(acne)的发生也与皮肤屏障功能受损密切相关。 Pappas 等[24] 的研究表明,痤疮患者的角质层中神经酰胺含量显著降低,组成也发生了变化,导致角质细胞间双层脂质膜的结构缺陷。 痤疮患者神经酰胺链长度的减少和不饱和脂肪酸水平的增加,可能导致皮肤屏障结构的不稳定,影响其保湿和保护功能。Zhou 等[25]研究发现,痤疮患者皮肤表面脂质组成发生了显著变化,尤其是甘油磷脂、脂肪酸和固醇脂水平增加,亚油酸、预醇脂和糖脂水平减少。 此外,磷脂酰丝氨酸水平的增加可能与炎症反应和细胞凋亡过程中的皮肤屏障损害有关,进一步加剧了痤疮患者的皮肤屏障问题。
Bolla 等[26]发现,痤疮丙酸杆菌感染可导致 Claudin⁃1 在角质层、颗粒层及棘层中表达降低,进而影响皮肤的屏障功能。 Dull 等[27]发现,Claudin⁃1 和 Occludin 的染色强度没有显著差异,但 Claudin⁃1 的染色模式在痤疮样本中发生了变化,表现为从基底层扩展至颗粒层,并在角质层中完全缺失。 这一分布模式的改变可能反映了 TJ 的破坏,导致皮肤屏障功能的下降。 提示皮肤屏障受损不仅在角质层,还涉及表皮其他层次。2. 3 慢性光化性皮炎 慢性光化性皮炎(chronic actinic dermatitis,CAD)患者存在皮肤屏障受损。 Harkins等[28]通过评估 CAD 患者皮损区域的 TEWL、角质层水分含量及神经酰胺酶的表达,发现这些患者的 TEWL明显升高,角质层的水合作用明显下降。
Tu 等[29]发现,UVB 和 UVA 辐射诱导 CAD 患者中 hsa⁃miR⁃31⁃3p 的表达增加,Claudin⁃1、FLG、LOR 和INV 的表达减少。 通过双荧光素酶报告基因分析,进一步证实 hsa⁃miR⁃31⁃3p 能通过靶向 Claudin⁃1 的 3′UTR 区域,负向调控 Claudin⁃1 的表达,影响皮肤屏障功能。 Tu 等[30]进一步研究发现,表皮全层 Claudin⁃1 表达显著降低,导致 TJ 结构不完整,揭示皮肤屏障受损累及表皮全层,应分层修复。 研究还通过双荧光素酶报告基因分析发现,CAD 患者中长链非编码 RNA(LncRNA)WAKMAR2 可通过招募 c⁃Fos 蛋白增强 Claudin⁃1的表达,从而维持皮肤屏障功能。 高剂量的 UVB 辐射会降低 WAKMAR2 的表达,进而减少 Claudin⁃1 的表达,导致皮肤屏障功能受损。
2. 4 银屑病 银屑病(psoriasis,PSO)是一种常见的慢性炎症性皮肤病。 Maroto⁃Morales 等[31] 发现,PSO 皮损部位的 TEWL 显著增加,角质层含水量降低,且未受累皮肤也表现出类似但较轻的屏障功能异常。 Yuki等[32]通过共聚焦拉曼光谱等非侵入性技术进一步证实,PSO 皮损的角质层结构紊乱,细胞间脂质排列异常,导致渗透屏障功能下降。
赵京霞等[33]研究发现,PSO 皮损中位于表皮全层的 Claudin⁃1 表达显著降低,导致 TJ 结构破坏,表皮通透屏障功能障碍。 提示皮肤屏障修复应兼顾表皮全层。 陈卫丰[34]的研究表明,在 PSO 皮损中,位于颗粒层、棘层及基底层的 Claudin⁃7 mRNA 和蛋白表达均显著降低,其可能通过破坏 TJ 完整性促进 T 淋巴细胞(如CD3+T 细胞)浸润,加剧局部炎症反应。2. 5 敏感性皮肤 敏感性皮肤(sensitive skin,SS)是一种皮肤综合征,表现为在外界微小刺激下,皮肤出现阵发性或周期性的灼热感、阵发性发红、刺痛、瘙痒及紧绷感,伴或不伴持续性红斑[35] 。 现有研究表明,SS的发生涉及皮肤屏障功能损伤、神经血管反应和固有免疫炎症的相互作用,是一个复杂的病理过程[36] 。 Lyu等[37]的研究显示,SS 的 TEWL 增加,角质层含水量降低。 Richters 等[38]发现,与正常皮肤相比,SS 中 Cer 及脂肪酸含量存在不同程度的减少。
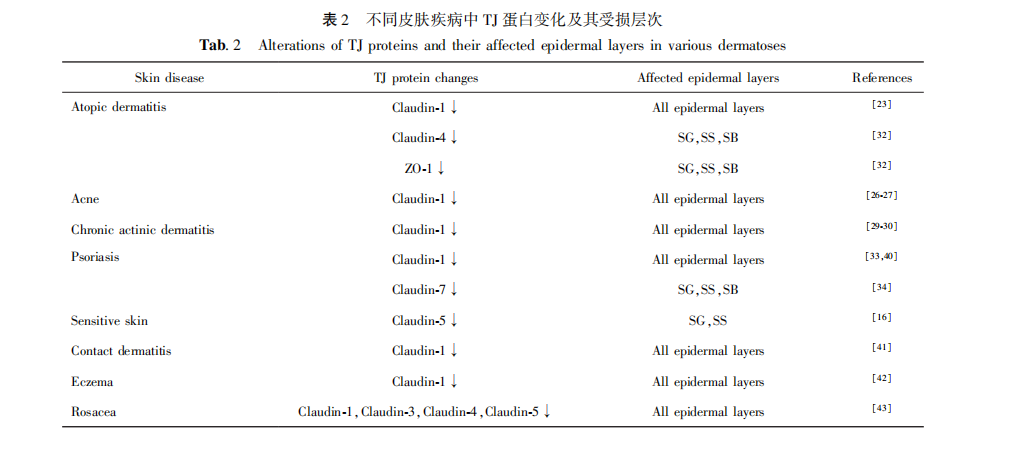
笔者团队研究[16]发现,SS 中位于颗粒层、棘层的 Claudin⁃5 mRNA 表达水平显著降低,导致 TJ 结构不完整,皮肤屏障完整性破坏,揭示了 Claudin⁃5 在 SS 发生中的关键作用。 Claudin⁃5 的缺失还累及颗粒层、棘层及基底层,提示修复皮肤屏障是治疗 SS 的基础,并应兼顾表皮多个层次。 笔者团队通过功效验证发现,上游miR⁃224⁃5p 可导致 Claudin⁃5 下调和表皮通透性屏障缺陷[39] 。 Claudin⁃5 的表达降低导致 MAPK 通路激活,下游促炎性细胞因子(如 IL⁃8、IL⁃23A)表达上调,参与 SS 炎症过程。 提示 SS 皮肤屏障受损累及不同层次。不同皮肤疾病中 TJ 蛋白变化及其受损层次,见表 2。
3 皮肤疾病及皮肤问题表皮屏障受损不同层次干预
3. 1 角质层受损的干预
3. 1. 1 补充角化套膜蛋白 笔者团队研究[44] 表明,青刺果油通过上调角化套膜蛋白 FLG、LOR、INV 的mRNA表达,可加速表皮通透屏障修复。 Zaniboni 等[45]通过动物模型实验发现,外用重组人 FLG 可显著提高皮肤中 FLG 的表达水平,增加角质层的水合能力,减少 TEWL,从而增强皮肤的保湿功能。 Lee 等[46] 研究表明,人参皂苷代谢产物原人参三醇(PPT)通过调节 MAPK/ AP⁃1 等通路可增强 AD 患者 FLG 表达,改善皮肤的水合状态,增强皮肤屏障功能。 陈志伟等[47]发现,含马齿苋、甘草等成分的润肤止痒膏对 AD 小鼠模型皮损有改善作用,可增加模型小鼠皮损中的 Cer 含量,促进 Flg 基因的表达,增加 FLG 蛋白含量,从而修复皮肤屏障。
3. 1. 2 修复细胞间质 笔者团队研究[48]发现,青刺果油可促进角质形成细胞 Cer 合成,上调酸性神经酰胺酶表达,增加表皮含水量和皮脂量。 许洁如等[49] 发现,含 Cer 的面霜或乳液可显著提高 SS 角质层含水量[使用后 4 周含水量从(144. 9 ± 24. 50) μs 升至(172. 5 ± 27. 70) μs],降低经表皮水分流失[ TEWL 从(21. 93 ± 2. 73) g / (m2 .h)降至(18. 93 ± 2. 98) g / (m2.h)],并减少红斑和干燥症状。 张路[50] 发现,中药参苓白术散可通过上调 Cer 合成酶,增加酰基 Cer 含量,从而修复皮肤屏障。 Elias 等[51] 通过局部应用含Cer、CHOL 和 FFA 的乳膏,以 3∶ 1∶ 1比例模拟天然脂质,发现乳膏可显著改善 AD 患者屏障完整性、水分含量及角质层结构。 表明修复细胞间质及细胞间质比例可改善角质层皮肤屏障。
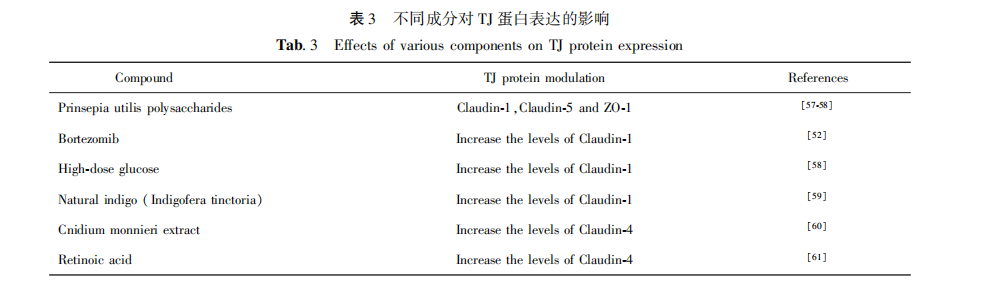
3. 2 颗粒层/ 棘层/ 基底层受损的干预 Kim 等[52]研究发现,使用蛋白酶体抑制剂硼替佐米可提高 AD 患者Claudin⁃1 的表达,结果显示皮肤屏障功能改善,AD 症状得到缓解。 Koda 等[53] 研究发现,黏多糖硫酸酯(MPS)可上调 Claudin⁃1 表达,恢复 TJ 结构和功能,改善 TEWL 和屏障完整性。 刘宇等[40] 发现,中药复方(如养血解毒方)可通过上调 PSO 患者 Claudin⁃1 及 Claudin⁃7 的表达修复 TJ 结构,从而抑制角质形成细胞异常增殖并改善屏障功能。 杨帆等[54] 研究表明,大米发酵滤液中的活性成分能显著上调角质形成细胞中Claudin⁃1、Claudin⁃4 和 Occludin 的 mRNA 和蛋白表达,强化 TJ 结构,从而改善皮肤屏障。 笔者团队通过在小鼠模型中诱导表皮屏障破坏,并局部应用青刺果多糖发现,青刺果多糖能显著提高 Claudin⁃1、Claudin⁃5 和ZO⁃1 的 mRNA 和蛋白表达水平[55] 。 Yang 等[56]发现,磷酸二酯酶⁃4(PDE⁃4)抑制剂克立硼罗可通过抑制炎症通路,显著上调 Claudin⁃8,增强 TJ 结构,修复皮肤屏障。 以上研究表明,上调 TJ 蛋白可改善颗粒层、棘层及基底层皮肤屏障。 不同成分对 TJ 蛋白表达的影响,见表 3。
4 总结
皮肤屏障不仅限于角质层,其完整性依赖于表皮多个层次结构与功能的协同,包括角化包膜与细胞间脂质,及颗粒层、棘层、基底层中的 TJ 蛋白。 多项研究表明,AD、痤疮、PSO、CAD 及 SS 等皮肤疾病和皮肤问题的屏障均表现为不同层次受损。
但迄今为止,传统干预多聚焦于角质层,缺乏对表皮不同层次屏障受损的分层检测及精准干预。 本文通过阐述不同皮肤疾病及皮肤问题表皮屏障分层受损机制,针对不同皮肤问题在不同时期存在的不同屏障受损情况,提出“表皮屏障受损及分层修复”新理念。 虽然目前的研究已经揭示了不同层次的损伤机制,但关于如何实现精准修复,仍需进一步探讨。 未来的研究将重点探索表皮屏障分层检测技术、渗透技术及分层修复产品的研究开发与应用,为表皮屏障受损提供更精准的策略。
利益冲突:所有作者均声明无利益冲突


本文转载于中国皮肤性病学杂志 2025 年 9 月第 39 卷第 9 期,不代表本网站赞同其观点和对其真实性负责,我们只作于阅读分享,非商业用途,如若侵权,请告知删除。

