一、概述
据中国国家癌症中心发布的数据,2022 年全国原发性肝癌发病人数 36.77 万,占全球病例的 42.5%,位列各种癌症新发患者数第 4 位、发病率位列第 5 位;2022 年因原发性肝癌死亡人数 31.65 万,死亡人数和病死率均位列第 2 位;人群肝癌 5 年相对生存率为 14.4%,诊断时为中期和晚期比例达 50%以上[1-3]。原发性肝癌主要包括肝细胞癌(hepatocellularcarcinoma , HCC )、 肝 内 胆 管 癌 ( intrahepaticcholangiocarcinoma,ICC)和混合型肝细胞癌-胆管癌(combinedhepatocellular-cholangiocarcinoma,cHCC-CCA)三种不同病理学类型,三者在发病机制、生物学行为、病理组织学、治疗方法以及预后等方面差异较大,其中 HCC 占 80%、ICC 占14.9%[4]。本指南中的“肝癌”仅指 HCC。
为推进我国肝癌诊疗规范化进程,原卫生部于 2011 年 10月首次发布《原发性肝癌诊疗规范(2011 年版)》。随着医学实践与科研进步,国家卫生健康委在 2017 年、2019 年、2021年及 2023 年完成四轮系统性修订,形成《原发性肝癌诊疗指南(2024 年版)》。该指南不仅系统整合了我国肝癌多学科诊疗(multi-disciplinary team,MDT)经验与科研成果,更为规范临床实践、优化医疗资源配置、提升患者生存质量提供了权威指导。自《原发性肝癌诊疗指南(2024 年版)》发布以来,全球在肝癌的诊断、分期及治疗方面出现了许多符合循证医学原则的高级别证据,尤其是适应中国国情的研究成果相继问世。为此,国家卫生健康委委托中华医学会肿瘤学分会,联合中国抗癌协会肝癌专业委员会、中国医师协会介入医师分会、中国医师协会外科医师分会和中华医学会超声医学分会等组织全国肝癌领域的多学科专家,结合肝癌临床诊治和研究的最新实践,再次修订并更新形成《原发性肝癌诊疗指南(2026年版)》(以下简称《指南》),以更好地规范肝癌的诊疗行为,反映肝癌诊治的最新进展,提升肝癌患者的总体生存(overallsurvival,OS)率,进一步推动落实并达成《“健康中国 2030”规划纲要》中实现总体癌症 5 年 OS 率提高 15%的目标。
证据评价与推荐意见分级、制定和评价方法学(grading ofrecommendations,assessment,development and evaluation,GRADE),是目前使用最广泛的证据评价和推荐意见分级系统[5]。GRADE 系统包括两部分,第一部分为证据评价,根据证据中的偏倚风险、不一致性、间接性、不精确性和发表偏倚,GRADE 系统将证据质量分为高、中、低和极低四个水平[6]。第二部分为推荐意见分级,GRADE 系统考虑医学干预的利弊平衡、证据质量、价值观念与偏好,以及成本与资源耗费等因素来制定推荐意见,并且将推荐意见分为强推荐和弱推荐(有条件推荐)两种[7]。医学干预的利弊差别越大,证据质量越高、价值观念与偏好越清晰越趋同、成本与资源耗费越小,则越应该考虑强推荐,反之,则应考虑弱推荐(有条件推荐)。本指南中的循证医学证据等级评估参照了上述 GRADE 分级的指导原则,采用了《牛津循证医学中心分级 2011 版》(OCEBMlevels of evidence)作为辅助工具来具体执行证据分级(证据等级 1~5)(附录 1)。在从证据转换成推荐意见的方法上,指南专家组主要参考了上述的 GRADE 对推荐意见分级的指导原则,同时结合了美国临床肿瘤学会(ASCO)指南的分级方案[8]对推荐意见分级作了相应的修改(附录 2)。最终将推荐强度分为三个等级,分别是强推荐、中等程度推荐和弱推荐(指南正文中分别用推荐 A、推荐 B 和推荐 C 表示)。强推荐(推荐 A)代表专家组对该推荐意见反映了最佳临床实践有很高的信心,绝大多数甚至所有的目标用户均应采纳该推荐意见。中等程度推荐(推荐 B)代表专家组对该推荐意见反映了最佳临床实践有中等程度的信心,多数目标用户会采纳该推荐意见,但是执行过程中应注意考虑医患共同决策。弱推荐(推荐 C)代表专家组对该推荐意见反映了最佳临床实践有一定的信心,但是应该有条件地应用于目标群体,强调医患共同决策。
二、预防、筛查和监测
(一)肝癌的预防预防和筛查监测是降低肝癌发病率和病死率的重要手段。据推算,若年龄标准化发病率(age-standardized incidence rates,ASIR)实现每年 2%~5%的降幅,到 2050 年全球可减少880~1730 万的新发肝癌病例,770~1510 万人将不会因肝癌死亡。全球 60%以上肝癌,可通过减少相关风险因素加以预防[9]。
接种乙型肝炎疫苗是预防乙型肝炎病毒(hepatitis B virus,HBV)感染最经济有效的方法。中国新生儿乙型肝炎疫苗已全部实施免费接种。各级医疗卫生机构应不断提升儿童乙型肝炎疫苗全程接种率和新生儿乙型肝炎疫苗首剂及时接种率。在12 h 内,尽早为乙型肝炎病毒表面抗原(hepatitis B virus surfaceantigen,HBsAg)阳性产妇所生婴儿接种乙型肝炎疫苗、注射乙型肝炎免疫球蛋白,加快全面消除 HBV 母婴传播。积极促进病毒性肝炎感染者早检测、早发现。针对重点地区和重点人群,探索通过健康体检、自我检测等方式,提高病毒性肝炎检测发现率和诊断率。医疗机构动员符合治疗条件的患者接受规范抗病毒治疗[10],并提供随访及相关不良临床结局监测等服务,不具备条件的要及时转诊。为病毒性肝炎患者及其家属提供健康教育和咨询服务,提高符合抗病毒治疗患者的治疗率、治疗依从性和治疗效果。在华东、华南等地区气候温暖湿润区域,积极防范黄曲霉毒素和蓝藻毒素暴露,注意粮油食品干燥和通风保存、避免木质厨具、餐具霉变。倡导通过饮食调整、运动锻炼等生活方式干预贯穿代谢功能障碍相关脂肪性肝病(metabolic dysfunction-associated fatty liver disease,MAFLD)治疗的全过程,提升 MAFLD 的分层管理和治疗能力及水平。卫生健康、中医药、疾控等部门应坚持经常性与集中性宣传教育相结合,积极宣传肝癌防治知识,倡导不吸烟、限制饮酒、合理膳食、科学运动等健康理念,提高科学健康知识的传播力和可及性。
(二)肝癌中、高风险人群的筛查和监测
由我国学者研发的适用于多种慢性肝病和多种族的肝癌风险评估模型 aMAP 评分(age-male-albi-platelets score),可便捷地将肝病人群分为肝癌低风险(aMAP 评分 0~50 分)、中风险(aMAP 评分 50~60 分)和高风险(aMAP 评分 60~100 分)人群,各组人群肝癌的年发生率分别为 0~0.2%、0.4%~1.0%和 1.6%~4.0%[11](证据等级 2,推荐 B)。此外,基于多变量纵向数据(aMAP 评分和 AFP)和循环游离 DNA(cell-freeDNA,cfDNA)特征构建的两种新型肝癌风险评估模型aMAP-2 和 aMAP-2 Plus,可进一步识别出肝癌年发生率高达12.5%的超高风险人群[12]。肝癌早期预警模型(ALARM),可提前 3~12 个月预警约 95%肝癌的发生[13](证据等级 2,推荐B)。
对肝癌的中、高风险人群(aMAP 评分 50~100 分)筛查与监测[超声检查(常规彩色多普勒超声)联合血清甲胎蛋白(alpha-fetoprotein,AFP)、异常凝血酶原(protein induced byvitamin K absence/antagonist-II , PIVKA-II 或 des-gammacarboxyprothrombin,DCP)检测],有助于肝癌的早期发现、早期诊断和早期治疗[14],同时可以显著降低肝癌病死率[15(] 证据等级 1,推荐 A)。肝癌的中、高风险人群快速、便捷识别是实施大范围肝癌筛查的前提,而对人群肝癌风险的分层评估是制定不同肝癌监测策略的基础。在我国,肝癌的中、高风险人群主要包括:具有 HBV 和(或)丙型肝炎病毒(hepatitis Cvirus,HCV)感染、过度饮酒、MAFLD、饮食中黄曲霉毒素B1 的暴露、其他各种原因引起的肝硬化及有肝癌家族史等人群,尤其年龄>40 岁的男性[9]。HBsAg 阴性但乙型肝炎核心抗体(hepatitis B core antibody,HBcAb)阳性的患者也应纳入肝癌中、高风险人群的筛查范围。加大中、高风险人群检测发现力度,建议 18 岁以上人群终生至少进行 1 次乙肝检测。
MAFLD 是我国常见的慢性进展性肝病,应该加强筛查和防治。MAFLD 的诊断基于以下 3 个标准:影像学诊断脂肪肝和/或肝活检发现≥5%肝细胞大泡性脂肪变性;存在 1 项及以上代谢综合征组分;排除过量饮酒(每周乙醇摄入量男性>210g,女性>140g)。能量密集型饮食和久坐少动生活方式及其催生的肥胖、代谢综合征、2 型糖尿病是 MAFLD 的主要危险因素。MAFLD 患者应该筛查并监测肝纤维化,合并进展期纤维化的 MAFLD 患者应该筛查肝癌,明确诊断肝硬化时还应筛查食管静脉曲张和肝脏失代偿事件[16]。
肝癌中、高风险人群应至少每隔 6 个月进行 1 次肝癌监测[11(] 证据等级 2,推荐 A);对于肝癌超高风险人群,每隔 6~12个月进行 1 次增强影像学检查[如增强磁共振成像(magneticresonance imaging,MRI)]加强监测,有助提高早期肝癌检出率。
肝癌筛查应重视将肝癌风险预测评分作为有效工具,在政府主导下,多方参与、“三医”联动、资源下沉,根据各地发病情况及当地资源开展大规模的社区、医院一体化的精准筛查新模式(早筛查、早预防、全程管理)[17](附录 3),从而有效提高肝癌早期诊断率,降低病死率。
要点论述:
(1)预防、筛查和监测是降低肝癌发病率和病死率的重要手段。
(2)接种乙型肝炎疫苗是预防 HBV 感染最经济有效的方法。
(3)为病毒性肝炎患者及其家属提供健康教育和咨询服务,提高符合抗病毒治疗人群的治疗率、治疗依从性和治疗效果。
(4)倡导通过饮食调整、运动锻炼等生活方式干预贯穿MAFLD 治疗的全过程,提升 MAFLD 的分层管理和治疗能力及水平。
(5)借助肝脏超声检查联合血清 AFP、PIVKA-II 进行肝癌的早期筛查,建议对肝癌的中、高风险人群(aMAP 评分50~100 分)至少每隔 6 个月进行 1 次筛查。
三、诊断
(一)肝癌的影像学诊断各种影像学检查手段各有特点,应该强调综合应用、优势互补、全面评估。
- 超声
超声检查具有便捷、实时、无创和无辐射等优势,是临床上最常用的肝脏影像学检查方法。
灰阶超声检查可以用于检出肝内占位性病变,鉴别其是囊性或实性,初步判断良性或恶性。典型肝癌灰阶超声表现为肝内实性占位,圆形或椭圆形,周边常可见低回声的声晕。小肝癌有时内部可见高回声区,这是肿瘤部分脂肪变的结果。灰阶超声还可观察到合并肝硬化的表现,如肝脏体积缩小、肝表面凸凹不平及门静脉高压等。少数弥漫型肝癌与肝硬化难以区分。同时,灰阶超声检查可以初步判断是否有肝内转移灶、肝内血管及胆管侵犯情况等。肝内转移灶多表现为肝内肿块周边或肝内其他部位出现大小不等的实性结节。门静脉、肝静脉及胆管癌栓表现为管腔内实性回声。癌栓完全充满门静脉管腔时周边可出现细小侧支循环形成,呈“蜂窝样”改变。肝癌直接侵犯周邻脏器如胆囊、右肾时,灰阶超声也可出现相应影像学改变。
彩色多普勒血流成像可以观察病灶血供状况,辅助判断病灶良恶性,显示病灶与肝内重要血管的毗邻关系以及有无肝内血管侵犯(证据等级 2,推荐 B)。肝癌在彩色多普勒血流成像上表现为病灶内部血流信号增加。脉冲多普勒检测在病灶内部可见动脉性血流信号,阻力指数多>0.6。门静脉、肝静脉及胆管出现癌栓时可在癌栓内检出动脉性血流信号。超声造影检查可以实时动态观察肝肿瘤血流灌注的变化,鉴别诊断不同性质的肝脏肿瘤[18-24](证据等级 2,推荐 A)。超声造影剂多使用微泡造影剂经外周静脉注射,微泡内部为惰性气体,其安全性高,过敏反应极少见。目前常用超声造影剂有注射用六氟化硫微泡和注射用全氟丁烷微球。前者为纯血池造影剂,可用于血管相成像;后者可被 Kuppfer 细胞吞噬,形成血管后相图像。血管相阶段包括动脉期(注射造影剂 30 s以内)、门静脉期(31~120 s)、延迟期(>120 s)。血管后相阶段一般定义为造影剂注射 10 min 后。典型肝癌超声造影多表现为病灶动脉期非环形高增强,增强时间早于病灶周围肝实质,门静脉或延迟期减退为低增强,即“快进快出”增强模式[23-24](证据等级 1,推荐 A)。与 ICC 和肝转移癌比较,肝癌造影剂廓清多出现于造影剂注射 60 s 后且廓清较轻微,而前二者多出现于 60 s 内且廓清更显著[25]。肝癌超声造影表现与病灶大小和分化程度相关,直径>3.0 cm 的肝癌多表现为上述典型增强模式,但少数<2.0 cm 者超声造影表现趋于不典型,高分化者造影剂廓清慢而低分化者廓清较快。
超声造影可用于区分再生结节、低度异型增生、高度异型增生、早期肝癌及进展期肝癌等不同阶段[26](证据等级 2,推荐 B)。有肝癌中、高风险的患者推荐采用超声造影肝脏影像报 告 与 数 据 系 统 ( CEUS liver imaging reporting and datasystem,CEUS LI-RADS)提高肝癌诊断的特异性[27](证据等级 2,推荐 A)。CEUS LI-RADS 诊断肝癌的符合率在 LR-3 类为 14%~39%,LR-4 类为 68%~86%,LR-5 类为 95%~98%。因此,LR-5 类病灶基本可以临床诊断为肝癌[26,28]。
肝癌在超声造影延迟期或血管后相多表现为低增强,与周围肝实质分界明显。因此超声造影可用于肝内多发微小病灶的检出[17](证据等级 2,推荐 B)。当肝内病灶延迟期或血管后相表现为低增强时,可在 10 min 后再次注射超声造影剂,观察病灶动脉期有无增强,进而判断病灶的有无及性质。血管后相造影剂(如注射用全氟丁烷微球)因为显影时间长(30 min至 2 h),尤其适合用于病灶的检出[24,29(] 证据等级 2,推荐 B)。超声造影检测肝癌病灶大小、数目、肝内脉管转移的能力与动态增强计算机断层成像(computed tomography,CT)或 MRI扫描的能力相近,因此也可以作为肝癌分期诊断的重要补充。超声造影可用于肿瘤消融的术前规划、术中实时引导、消融后即刻评估局部疗效;消融后即刻评估有助于迅速发现未完全消融的残留病灶,及时补充治疗[23,30(] 证据等级 2,推荐 A)。
超声造影也可用于肝癌消融术中及术后并发症的观察,如肝表面穿刺点的活动性出血,术后肝脓肿、胆汁瘤、动脉瘤、肝实质缺血性梗死等的识别。超声造影同样适用于消融术后的影像学随访,可在早期识别局部肿瘤进展或肝内其余部位复发,为疾病控制争取时间[31](证据等级 2,推荐 A)。注意肝癌残留或复发不一定会出现门脉期或延迟期造影剂廓清,此外还要与治疗区域周边的反应性充血相鉴别。
定量超声造影可测量造影剂到达时间、达峰时间、渡越时间、峰值强度、血流灌注量等指标,可用于评估系统抗肿瘤治疗(化疗、靶向治疗、免疫治疗等)后的疗效以及早期预测患者对系统抗肿瘤治疗的反应性,辅助临床决策[32-33]。基于超声造影的超分辨超声成像技术,可更清晰显示肝癌微血管(直径可小至 0.05 mm),有望提高对肝癌的诊断及疗效评估能11力[34-35]
超声联合动态增强 CT、MRI 的影像导航技术,在肝癌精准定位中具有重要价值,尤其有助于常规超声检查难以显示的隐匿性肝癌的定位[30,36-37](证据等级 3,推荐 B)。超声融合影像导航在肝癌消融术前计划、术中监测及安全边缘判断、术后即刻评估疗效中也具有一定价值。融合导航中使用超声造影能进一步提高评估准确性[37-38]。
超声剪切波弹性成像可以定量测量肝肿瘤周边肝实质的纤维化/硬化程度,进一步评估肝脏储备功能[39-41(] 证据等级 3,推荐 B)。肝脏超声脂肪定量技术可定量分析并能以百分比形式显示肝脏脂肪含量,结合超声弹性等技术可评估 MAFLD 患者的肝脏状态,为 MAFLD 相关性肝癌的预警提供辅助信息[42-46]。
术中超声(超声造影)在肝外科手术中的应用也越来越普及,可敏感检出隐匿性微小病灶、判断手术切除范围和切缘情况[47]。高频超声有助于发现肝包膜下或位置较表浅的隐匿病灶[17]。超声影像组学对鉴别诊断肝癌、预测肝癌微血管浸润等生物学行为及选择治疗手段等有一定的意义[48]。通过融合患者临床和肿瘤影像信息,可建立肝肿瘤智能诊断和预测模型;有望为临床选择消融或手术治疗提供科学、合理决策[49-51]。肝脏超声检查受限于检查者的经验,MDT 的开展有助于超声检查者和术中超声操作者积累经验。
- CT 和 MRI
动态增强 CT、MRI 扫描是肝脏超声和(或)血清 AFP、PIVKA-II 筛查异常者明确肝癌诊断的首选影像学检查方法(附录 4)。肝脏动态增强 MRI 具有无辐射、组织分辨率高、多方位多序列动态增强成像等优势,且具有形态结合功能(包括扩散加权成像等)综合成像能力,成为肝癌临床检出、诊断、分期和疗效评价的优选影像技术。动态增强 MRI 对直径≤2.0cm 肝癌的检出和诊断能力优于动态增强 CT [52-53(] 证据等级 1,推荐 A)。动态增强 MRI 在评价肝癌是否侵犯门静脉、肝静脉主干及其分支,以及腹腔或腹膜后间隙淋巴结转移等方面,较动态增强 CT 具有优势12。
采用动态增强 MRI 扫描评价肝癌治疗疗效时:对于非放射治疗,包括局部治疗(如手术/介入/射频等)及全身系统治疗,可使用改良版的实体瘤疗效评价标准(modified responseevaluation criteria in solid tumor,mRECIST)结合 T2WI 及 DWI进行综合判断;对于内、外放射治疗,可采用 LI-RADS TRAv2024 评价标准,同时强调需结合 T2WI 及 DWI 进行综合判断[54]。
CT/MRI(非特异性钆类对比剂)动态增强三期扫描包括:动脉晚期(门静脉开始强化,通常注射对比剂后约 35 s 扫描)、门静脉期(门静脉已完全强化,肝静脉可见对比剂充盈,肝实质通常达到强化峰值,通常注射对比剂后 60~90 s 扫描)、延迟期(门静脉、肝静脉均有强化但低于门脉期,肝实质可见强化但低于门脉期,通常注射对比剂后 3 min 扫描)。肝细胞特异性 MRI 对比剂(钆塞酸二钠,Gd-EOB-DTPA)动态增强四期扫描包括:动脉晚期(同上)、门静脉期(同上)、移行期(肝脏血管和肝实质信号强度相同,肝脏强化是由细胞内及细胞外协同作用产生,通常在注射 Gd-EOB-DTPA 2~5 min 后扫描)、肝胆特异期(肝脏实质信号高于肝血管,对比剂经由胆管系统排泄,通常在注射 Gd-EOB-DTPA 12~20 min 后扫描;肝功能正常者、一般肝胆特异期 12~15 min 扫描,而肝功能明显降低者、一般只需延迟 20 min 即可)。
肝癌影像学诊断主要根据动态增强扫描的“快进快出”强化方式[55-57](证据等级 1,推荐 A)。动态增强 CT 和 MRI 动脉期(主要在动脉晚期)肝肿瘤呈均匀或不均匀明显强化,门静脉期和(或)延迟期肝肿瘤强化低于肝实质。“快进”为非环形强化,“快出”为非周边廓清。“快进”在动脉晚期观察,“快出”在门静脉期及延迟期观察。Gd-EOB-DTPA 通常在门静脉期观察“快出”征象,但移行期及肝胆特异期“快出”征象可以作为辅助恶性征象。
Gd-EOB-DTPA 增强 MRI 检查显示:肝肿瘤动脉晚期明显强化,门静脉期或移行期强化低于肝实质,肝胆特异期常呈明显低信号。但仍有 5%~12%分化较好的肝癌,尤其是直径≤2.0cm 的肝癌,肝胆特异期可见肿瘤部分呈吸收对比剂的稍高信号[58]。Gd-EOB-DTPA 增强 MRI 尤其适用于合并肝硬化的患者,同时有助于与高度异型增生结节等癌前病变相互鉴别[59]。
对于肿瘤直径≤2.0 cm 肝癌的诊断,强调尚需要结合其他影像征象(如包膜样强化、T2 加权成像中等信号和扩散受限等)及超阈值增长(6 个月内病灶最大直径增大 50%)进行综合判断[60](证据等级 3,推荐 B)。动态增强 MRI 扫描包膜样强化的定义为:光滑,均匀,边界清晰,大部分或全部包绕病灶,特别在门静脉期、延迟期或移行期表现为环形强化。
将影像学上测量直径≤1.0 cm 的肝癌定义为亚厘米肝癌(subcentimeter hepatocellular carcinoma,scHCC)。根据文献报道,scHCC 局部切除术后 5 年 OS 率为 97.3%,明显高于直径 1.0~2.0 cm 的肝癌(5 年 OS 率为 89.5%)[61]。在中、高风险人群中,排除 T2 极高信号血管瘤病灶及“靶征”病灶后,推荐使用 Gd-EOB-DTPA 增强 MRI 诊断 scHCC[62-67],其诊断敏感性为 72.1%(95%CI 64.8~78.5%)。诊断标准:动脉晚期强化+门脉或移行期廓清;如动脉晚期强化不理想者,建议需结合细胞外对比剂 MRI 增强进行综合评估[62-67](证据等级 2,推荐 B)。
目前 CT 平扫及动态增强扫描除应用于肝癌的临床诊断及分期外,也应用于肝癌局部治疗的疗效评价,特别是观察经动脉化疗栓塞(transarterial chemoembolization,TACE)后碘油沉积状况及肿瘤存活有一定优势,同时有助于决定是否需要再次 TACE 治疗[68-70]。基于术前 CT 的影像组学技术也可以用于预测首次 TACE 治疗的疗效[71]。同时,借助 CT 后处理技术可以进行三维血管重建、肝脏体积和肝肿瘤体积测量。三维可视化重建技术可以进行肝脏分叶分段处理,术前模拟手术,辅助医生制定最优手术方案。
基于肝癌动态增强 CT 和(或)MRI 信息,并结合临床数据挖掘建立融合模型有助于改善临床决策(患者治疗方案选择、疗效评价及预测等)[72]。对于术前预测肝癌微血管侵犯(microvascular invasion,MVI),影像学征象特异性高,但敏感性较低,人工智能(包括影像组学和生境分析等深度机器学习模型)是术前预测 MVI 的可能突破点[73-75](证据等级 3,推荐 B)。
- 数字减影血管造影
数字减影血管造影(digital subtraction angiography, DSA)是肝癌血管内介入治疗前必须进行的检查,常采用经选择性或超选择性肝动脉插管进行。DSA 检查可以清楚地显示肝动脉解剖和变异以及肿瘤血管、染色,明确肿瘤数目、大小及其血供丰富程度[76]。DSA 联合锥形束 CT(cone beam CT,CBCT)可更清楚显示肿瘤病灶、提高小肝癌的检出率,明确肿瘤供血动脉分支的三维关系、指导肿瘤供血动脉分支的超选择性插管[77](证据等级 2,推荐 A)。经肠系膜上动脉或脾动脉的间接门静脉造影,可以评价门静脉血流和门静脉主干或一级分支癌栓栓塞等情况。
- 核医学影像学检查
(1)正电子发射断层成像(positron emission tomography,PET):包括 PET/CT 和 PET/MR 融合影像。目前,PET 常用的 显 像 剂 为 氟 -18- 脱 氧 葡 萄 糖 ( 18F-flurodeoxyglucose ,18F-FDG),18F-FDG PET/CT 或 PET/MR 全身显像的优势在于:① 对肿瘤进行分期,通过一次检查能够全面评价有无淋巴结转移及远处器官的转移[78-79](证据等级 1,推荐 A);②再分期,因 PET 功能影像不受解剖结构的影响,可以准确显示解剖结构发生变化后或者解剖结构复杂部位的复发转移16灶[80](证据等级 2,推荐 B);③对于抑制肿瘤活性的靶向药物的疗效评价更加敏感、准确[81-82](证据等级 2,推荐 A);④指导放射治疗生物靶区的勾画、确定穿刺活检部位[80];⑤评价肿瘤的恶性程度和预后[83-85](证据等级 2,推荐 B)。18F-FDGPET 显像对肝癌诊断的敏感性和特异性有限,可作为其他影像学 检 查 的 有 益 辅 助 和 补 充 。 采 用 碳 -11 标 记 的 乙 酸 盐(11C-acetate)或胆碱(11C-choline)等显像剂 PET 显像可以提高对高分化肝癌诊断的敏感度,与 18F-FDG PET 显像具有互补作用[86-87]。镓-68(68Ge)或 18F 标记的成纤维细胞活化蛋白抑制剂(fibroblast activation protein inhibitor,FAPI)PET显像可有效提高对于肿瘤间质成分丰富的肝癌原发灶、转移灶的诊断灵敏度,对 18F-FDG PET 显像具有补充作用 [88-89](证据等级 3,推荐 C)。68Ge 标记的磷脂酰肌醇蛋白聚糖 3(glypican-3,GPC-3)PET/CT 显像由于肝脏本底背景低,有望提高肝癌的诊断及分期敏感度[90]。PET/MR 具有软组织分辨率高,且可行多参数成像的特点,对肝癌病灶显示更加清晰,同时因为没有 CT 辐射相较 PET/CT 的普适性更好。
(2)单光子发射计算机断层成像(single photon emissioncomputed tomography/CT,SPECT/CT):SPECT/CT 已逐渐替代 SPECT 成为核医学单光子显像的主流设备,选择全身平面显像所发现的病灶,再进行局部 SPECT/CT 融合影像检查,可以 同 时 获 得 病 灶 部 位 的 SPECT 和 诊 断 CT 图 像 ,99mTc-DP-FAPI SPECT/CT 显像可用于肝癌诊断[91]。
(二)肝癌的检验、检测
- 常规检验、检测
(1)血常规
了解有无贫血、肝癌破裂出血等可能。白细胞、血小板等早期无明显变化;晚期或合并严重肝硬化者,可出现白细胞、血小板减少,增加出血、感染等风险及严重程度。
(2)凝血功能检查
多个凝血因子在肝脏代谢,因此,当晚期肝癌出现肝功能障碍时,可出现凝血障碍和出血。
(3)尿常规
早期肝癌患者尿常规检查常无特殊;晚期肝癌致肝细胞明显损害或胆道系统阻塞时,尿胆红素可出现强阳性。
(4)粪隐血试验
部分患者可出现粪隐血试验阳性,可能与门静脉高压胃肠道黏膜瘀血、破损、溃疡有关。部分晚期患者可因门静脉高压致食管胃底曲张静脉破裂大量出血,粪便可呈红色,镜检可见血细胞。
(5)病毒性肝炎标志物
乙型肝炎和丙型肝炎与肝癌发生发展有密切关系。因此,检查肝炎病毒标志物,对临床诊断和治疗方式的选择有重要意义。HBV 血清学标志物通常包括:乙型肝炎病毒表面抗原(hepatitis B virus surface antigen,HBsAg)、乙型肝炎病毒表面抗体(antibody to hepatitis B virus surface antigen,HBsAb)、乙型肝炎病毒 e 抗原(hepatitis B virus e antigen,HBeAg)、乙型肝炎病毒 e 抗体(antibody to hepatitis B virus e antigen,HBeAb)、HBcAb。HCV 的核心确证指标是血清 HCV RNA。
(6)生化常规
肝癌早期肝功能可无明显变化,但随肿瘤进展,可出现肝功能受损表现,如转氨酶升高、白蛋白下降、胆红素升高等。
(7)HBV-DNA
检测HBV复制情况,抗病毒治疗应覆盖全程。尽管抗HBV治疗无法完全避免肝癌发生,但可显著降低肝癌发生风险。
(8)自身抗体
自身抗体是自身免疫性肝病分型诊断的首要依据,不同亚型有其特征性自身抗体,部分抗体具有确诊价值,部分为筛查/辅助诊断价值,临床需结合抗体谱+肝功能+免疫球蛋白综合判断,核心抗体包括:抗核抗体、抗平滑肌抗体、抗线粒体抗体、肝肾微粒体抗体等。
- 肿瘤标志物
血清AFP是当前诊断肝癌和疗效监测常用且重要的指标。血清 AFP≥400 ng/mL,在排除妊娠、慢性或活动性肝病、生殖腺胚胎源性肿瘤以及其他消化系统肿瘤后,高度提示肝癌;而血清 AFP 轻度升高者,应结合影像学检查或作动态观察,并与肝功能变化对比分析,有助于诊断。PIVKA-Ⅱ和血浆游离微小核糖核酸(microRNA)[92]也可以作为肝癌早期诊断标志物,特别是对于血清 AFP 阴性人群。血清甲胎蛋白异质体(lensculinaris agglutinin-reactive fraction of AFP,AFP-L3)(比率)在肝癌时增高,肝脏良性疾病及导致 AFP 升高的其他疾病一般不增高,可用于鉴别诊断。基于性别、年龄、AFP、PIVKA-II和 AFP-L3 构建的 GALAD 模型在诊断早期肝癌的敏感性和特异性分别为 85.6%和 93.3%,有助于肝癌的早期诊断[93](证据等级 1,推荐 A)。目前已有基于中国人群大样本数据的优化的类 GALAD 模型(C-GALAD、GALAD-C、C-GALAD Ⅱ等)用于肝癌的早期诊断。另外,基于性别、年龄、AFP、PIVKA-II构建的简化的 GAAD 模型[94]及 ASAP 模型[95]与 GALAD 模型诊断效能类似(证据等级 1,推荐 A)。基于 7 个 microRNA组合的检测试剂盒诊断肝癌的敏感性和特异性分别为 86.1%和 76.8%,对 AFP 阴性肝癌的敏感性和特异性分别为 77.7%和84.5%[92](证据等级 1,推荐 A)。
近 年 来 , “ 液 体 活 检 ” 包 括 循 环 游 离 微 小 核 糖 核 酸(circulating cell-free microRNA)、循环肿瘤细胞(circulatingtumor cell,CTC)[96]、cfDNA[97]、循环肿瘤 DNA(circulatingtumor DNA,ctDNA)[98-99]、游离线粒体 DNA、游离病毒 DNA和细胞外囊泡等,在肿瘤早期诊断和疗效评价等方面展现出重要价值(附录 5)。
(三)肝癌的穿刺活检
具有典型肝癌影像学特征的肝占位性病变,符合肝癌诊断标准的患者,通常不需要以诊断为目的的肝病灶穿刺活检[100-102](证据等级 1,推荐 A),特别是对于具有外科手术指征的肝癌。能够手术切除或准备肝移植的肝癌,不建议术前行肝病灶穿刺活检,以减少肝肿瘤破裂出血、播散风险。对于缺乏典型肝癌影像学特征的肝占位性病变,肝病灶穿刺活检可获得明确的病理诊断。转化治疗手术前,为评估手术安全性,观察肿瘤微环境中炎症细胞和淋巴细胞浸润,评估肝细胞坏死情况,必要时也可行肝穿刺活检。肝病灶和瘤周穿刺活检可以明确病灶性质及肝癌分子分型 以及瘤周微环境,为明确肝病病因、指导治疗、判断预后和进行研究提供有价值的信息,故应根据肝病灶穿刺活检的患者受益、潜在风险以及医师操作经验综合评估穿刺活检的必要性。
肝病灶穿刺活检通常在超声或 CT 引导下进行,必要时可进行超声造影以提高穿刺阳性率,可以采用 18 G 肝穿刺空芯针活检获得病灶组织。其主要风险是可能引起出血和肿瘤针道种植转移。因此,术前应检查血小板和出凝血功能,对于有严重出血倾向的患者,应避免肝病灶穿刺活检。穿刺路径应尽可能经过正常肝组织,避免直接穿刺肝脏表面结节。穿刺部位应选择影像检查显示肿瘤活跃的肿瘤内和肿瘤旁。对于肝门部淋巴结及病灶,常规方法无法穿刺的,可考虑行超声内镜引导下穿刺。对于常规超声或 CT 引导困难的,可以考虑采用超声造影引导或超声融合导航下、经超声内镜或经腹腔镜等方法进行。另外,受病灶大小、部位深浅等多种因素影响,肝病灶穿刺病理学诊断也存在一定的假阴性率,特别是对于直径≤2 cm的病灶,假阴性率较高。因此,肝病灶穿刺活检阴性结果并不能完全排除肝癌的可能,仍需观察和定期随访。对于活检组织取样过少、病理结果不支持但临床上高度怀疑肝癌的患者,可以在影像引导下重复进行肝病灶穿刺活检或者密切随访。
要点论述:
(1)动态增强 CT/MRI 扫描、Gd-EOB-DTPA 动态增强MRI 检查以及超声造影是肝脏超声检查和(或)血清 AFP、PIVKA-II 筛查异常者明确诊断的影像学检查方法。
(2)肝癌影像学诊断依据主要根据“快进快出”的强化方式。
(3)肝脏动态增强 MRI 检查是肝癌临床诊断、分期和疗效评价的优选影像手段。
(4)PET/CT 扫描有助于对肝癌进行分期及疗效评价。
(5)血清 AFP 是诊断肝癌和疗效监测常用且重要的指标。对血清 AFP 阴性人群,可以借助 PIVKA-II、基于 7 个microRNA 组合的检测试剂盒等进行早期诊断。
(6)具有典型肝癌影像学特征的肝占位性病变,符合肝癌诊断标准的患者,通常不需要以诊断为目的的肝病灶穿刺活检。
(四)肝癌的病理学诊断
- 肝癌病理学诊断术语
原发性肝癌:统指起源于肝细胞和肝内胆管上皮细胞的恶性肿瘤,主要包括 HCC、ICC 和 cHCC-CCA[103]。
(1)HCC
是指肝细胞发生的恶性肿瘤。不推荐使用“肝细胞肝癌”或“肝细胞性肝癌”的病理诊断名称[104]。
(2)ICC
是指肝内胆管衬覆上皮细胞发生的恶性肿瘤,以腺癌最为多见。2019 年第五版《WHO 消化系统肿瘤分类》(WHO 分类)不推荐使用胆管细胞癌(cholangiocellular carcinoma)和细胆管细胞癌(cholangiolocellular carcinoma)的病理诊断名称[103]。
(3)cHCC-CCA
是指在 1 个肿瘤结节内同时存在 HCC 和 ICC 两种肿瘤成分,并分别表达各自相应的免疫表型,同时排除碰撞瘤。
- 肝癌病理诊断规范
肝癌病理学诊断规范由标本前处理、标本取材、病理检查和病理报告等部分组成。
(1)标本处理要点
①手术医师应在病理检查申请单上明确标注送检标本的种类、部位和数量,是否曾接受转化/新辅助治疗以及方案与周期等信息,对手术切缘和重要病变可以用染料或缝线加以标记;②应在标本离体后 30 min 内切开固定。组织库留取标本时应在病理科的指导下进行,以保证取材的准确性,并应首先满足病理诊断的需要;③10%中性缓冲福尔马林溶液固定12~24 h。
(2)标本取材要点
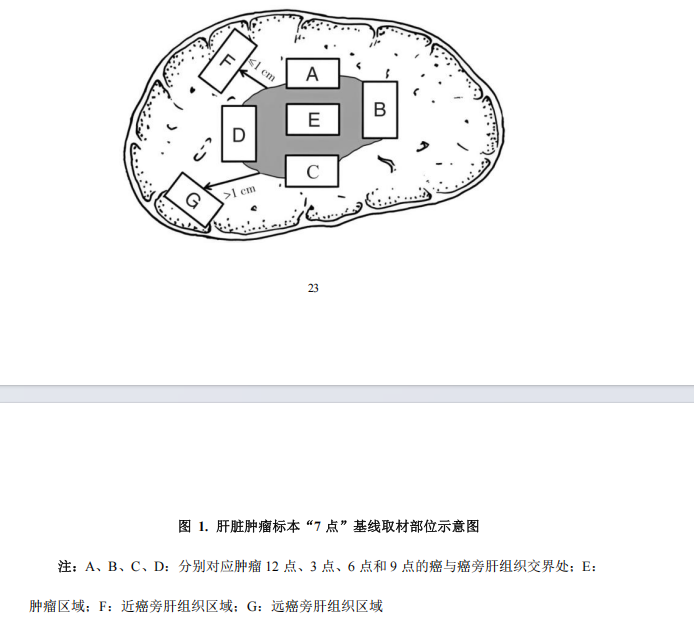
肝癌周边交界区域是肿瘤生物学行为的代表性区域。为此要求采用“7 点”基线取材法(图 1),在肿瘤的 12 点、3 点、6点和 9 点位置上于癌与癌旁肝组织交界处按 1∶1 取材;在肿瘤内部至少取材 1 块;对距肿瘤边缘≤1 cm(近癌旁)和>1 cm(远癌旁)范围内的肝组织分别取材 1 块。距肿瘤最近切缘及另送组织需分别取材,实际取材的部位和数量还需根据肿瘤的直径和数量酌情增加取材[105-106]。肿块型和混合型 ICC 标本取材时参照“7 点”基线取材法;管周浸润型 ICC 标本取材时,推荐沿受侵胆管壁纵向剖开取材,并对胆管切缘进行取材。对单个肿瘤最大直径≤3 cm 的小肝癌,应全部取材检查(证据等级3,推荐 A)。
- 肝癌病理检查要点
(1)大体标本观察与描述对送检的所有手术标本全面观察,重点描述肿瘤的大小、数量、颜色、质地、与血管和胆管的关系、包膜状况、周围肝组织病变、肝硬化类型、肿瘤至切缘的距离以及切缘情况等。HCC 大体分型参见附录 6。ICC 大体分为肿块型、管周浸润型和混合型(肿块形成合并管周浸润)。
(2)显微镜下观察与描述对所有取材组织全面观察,原发性肝癌的病理诊断可参照WHO 分类[103],重点描述以下内容:①HCC 常见组织学类型包括细梁型、粗梁型、假腺管型、团片型。特殊组织学类型包括纤维板层型、硬化型、透明细胞型、富脂型、嫌色型、巨梁型、富于中性粒细胞型、富于淋巴细胞型和未分化型等。双表型 HCC 在临床、影像学、血清学、癌细胞形态和组织结构上均表现为典型的 HCC 特征,但免疫组化标记显示同时表达肝细胞性标志物和胆管上皮标志物,这类 HCC 的侵袭性较强[107],对瑞戈非尼治疗可能敏感[108]。②HCC 的分化程度可以采用国际上常用的 Edmondson-Steiner 四级(Ⅰ~Ⅳ)分级法或WHO 推荐的高、中、低分化,若有多种分化成分,应报告主要成分和最差成分的分级及所占比例。③ICC 的组织学亚型主要包括大胆管型和小胆管型[109]。大胆管型 ICC 起源于肝内隔胆管以上至邻近肝门区之间较大的胆管,腺管口径大而不规则,可见黏液;小胆管型 ICC 起源于小叶间胆管及隔胆管,腺管口径较小,排列较规则。部分小胆管型 ICC 还可表现为细胆管癌和胆管板畸形型等特殊组织学亚型,其中细胆管癌起源于赫令管或细胆管,癌细胞多呈小立方形,在透明变性的胶原纤维间质内呈松散的成角小导管或分支状排列;胆管板畸形型 ICC 的肿瘤腺管多呈不规则囊状扩张,管腔内可见乳头状突起。此外,尚存在多种其他少见类型的 ICC,如腺鳞癌、鳞状细胞癌、黏液腺癌、印戒细胞癌、透明细胞癌、淋巴上皮样癌及肉瘤样癌等。有研究显示,大胆管型 ICC 的生物学行为及基因表型特征与其他类型 ICC 存在差异,其临床预后相对较差。病理诊断及鉴别诊断应在综合患者临床特点、大体类型、细胞形态、组织结构、免疫表型及分子变异等信息的基础上进行,并建议采用 AJCC/TNM 分期系统完成病理分期。④肝癌的生长方式包括癌周浸润形式(膨胀式/侵袭式)、MVI、卫星灶、包膜侵犯或突破等。⑤对于手术切除肝癌标本,可以评估三级淋巴结构(tertiary lymphoid structure,TLS),包括 TLS的成熟度、数量及位置。TLS 是后天形成于非淋巴组织中的高度结构化的免疫细胞聚集体[110],主要分为两种类型:不成熟TLS(包括淋巴细胞聚集成结节状和初级淋巴滤泡形成)和成熟 TLS(次级淋巴滤泡形成)[111]。可着重对全部切片中成熟TLS 的数量进行计数,并注明 TLS 存在的部位,特别是肿瘤内的 TLS 与肝癌患者的预后相关[112-113],并可根据临床需要对TLS 的细胞组分进行相应免疫组化标记。⑥慢性肝病评估,肝癌常伴随不同程度的慢性病毒性肝炎或肝硬化等致病因素,推荐采用较为简便的 Scheuer 评分系统和中国慢性病毒性肝炎组织学分级和分期标准[114-116],并注意 MALSD 等慢性肝病的诊断和鉴别诊断。
(3)MVI 诊断
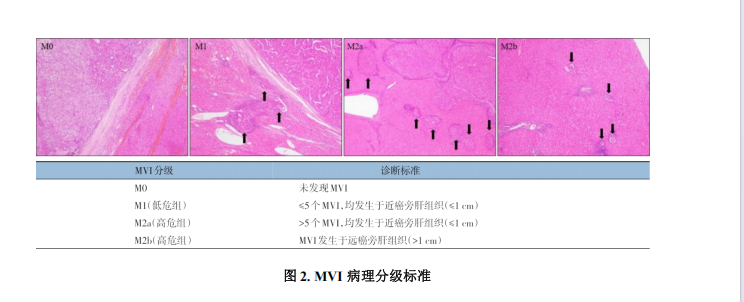
MVI 是指在显微镜下于内皮细胞衬覆的脉管腔内见到的癌细胞巢团[106],HCC 以门静脉分支侵犯(含包膜内血管)最为多见,ICC 可有淋巴管侵犯。MVI 病理分级方法主要针对HCC[117]:M0:未发现 MVI;M1(低危组):≤5 个 MVI,且均发生于近癌旁肝组织(≤1 cm);M2(高危组):M2a 定义为>5个近癌旁 MVI,且无远癌旁 MVI;M2b 定义为 MVI 发生于远癌旁肝组织(>1 cm)(图 2)。MVI 各组患者的术后复发转移风险依次增加,临床预后依次降低。MVI 和卫星灶可视为肝癌发生肝内转移过程的不同演进阶段,当癌旁肝组织内的卫星灶与 MVI 难以区分时,可一并计入 MVI 病理分级。MVI 是评估肝癌术后复发转移风险和选择治疗方案的重要病理依据[104,106],应作为组织病理学常规诊断指标。MVI 病理分级是建立在“7 点”基线取材的基础上评估的,当送检标本不能满足“7点”基线取材时,应在 MVI 分级时加以说明。在诊断 ICC 时建议报告有无脉管(血管/淋巴管)侵犯(证据等级 2,推荐 A)。
(4)cHCC-CCA 诊断
研究表明,肿瘤成分比例是影响 cHCC-CCA 生物学行为的重要病理因素。当某一主要肿瘤成分比例>70%,次要肿瘤成分比例≤30%时,则主要肿瘤成分在肿瘤标志物表达、生长方式、术后抗复发疗效和预后等方面会表现出更显著的优势效应;而当肿瘤成分比例接近时,则 cHCC-CCA 会兼有 HCC 和ICC 的临床病理特征[118]。为此建议在诊断 cHCC-CCA 时,对各肿瘤成分的比例情况、组织学分级和亚型分型等进行评估,并对 MVI 分级、淋巴管侵犯及淋巴结转移成分进行说明,以供临床制定诊疗方案时参考。对于初诊为 cHCC-CCA 的肿瘤标本可酌情增加取材数量和范围,以进一步核实各肿瘤成分的占比情况。
- 鉴别诊断
肝癌免疫组化检查的主要目的是:首先是肝细胞肿瘤与非肿瘤之间的鉴别;肝细胞良性、恶性肿瘤之间的鉴别;其次是原发性肝癌与肝转移瘤之间的鉴别;以及 HCC 与 ICC 以及其他特殊类型的肝脏肿瘤之间的鉴别。由于肝癌组织学类型的高度异质性,现有的肝癌标志物在诊断特异性和敏感性均存在某种程度的不足,常需要合理组合、客观评估,有时还需要与其他系统肿瘤的标志物联合使用(证据等级 2,推荐 A)。
(1)HCC 常用的免疫组化标志物
以下标志物对肝细胞标记阳性,有助于提示肝细胞来源的肿瘤,但不能作为区分肝细胞良性、恶性肿瘤的依据。①精氨酸酶-1(arginase-1,Arg-1):肝细胞胞浆/胞核染色。②肝细胞抗原(hepatocyte paraffin 1,HepPar-1):肝细胞胞浆染色。③肝细胞膜毛细胆管缘特异性染色抗体:如分化抗原(cluster ofdifferentiation,CD)10、多克隆性癌胚抗原(polyclonalcarcinoembryonic antigen,pCEA)和胆盐输出泵蛋白(bile saltexport pump,BSEP)等抗体可以特异性标记肝细胞膜的毛细胆管面,有助于确认肝细胞性肿瘤。
以下标志物有助于肝细胞良性、恶性肿瘤的鉴别。①谷氨酰胺合成酶(glutamine synthetase,GS):HCC 多呈弥漫性胞浆强阳性;部分类型的肝细胞腺瘤,特别是β-连环蛋白(β-catenin)突变型肝细胞腺瘤常表现为弥漫阳性;在高级别异型增生结节为中等强度灶性染色,阳性细胞数通常<50%;在肝局灶性结节性增生呈特征性的不规则“地图样”染色;在正常肝组织仅中央静脉周围的肝细胞染色,这些特点有助于鉴别诊断。②GPC-3 [119]:HCC 细胞浆及细胞膜染色。GPC-3 是 HCC治疗相关靶点,因而可对 GPC-3 染色模式进行判读,包括染色定位、染色百分比、染色强度(如膜 80%+++)。基于 Glypican3 的检测试剂盒(免疫组织化学法)于 2014 年 8 月 13 日获国家食品药品监督管理局颁发的三类医疗器械注册证,是我国首个获批完全自主产权的肿瘤病理诊断试剂盒。该试剂盒主要应用于肝癌的病理诊断,尤其是肝癌疑难病例的良恶性鉴别诊断以及 AFP 阴性肝癌的临床诊断。该试剂盒的特异性和敏感性分别达到 97.7%和 73.8%。③热休克蛋白 70(heat shock protein70,HSP70):HCC 细胞浆或细胞核染色。④CD34:CD34 免疫组化染色虽然并不直接标记肿瘤细胞,但可以显示不同类型肝脏肿瘤的微血管密度及其分布模式特点:如 HCC 为弥漫型、ICC 为稀疏型、肝细胞腺瘤为斑片型或弥漫型、肝局灶性结节性增生为条索型等,结合肿瘤组织学形态有助于鉴别诊断
(2)ICC 常用的免疫组化标志物
①ICC 通用免疫组化标志物:细胞角蛋白 7(cytokeratin 7,CK7)、细胞角蛋白 19(cytokeratin 19,CK19)、黏蛋白 1(mucin1,MUC1)、MOC31。②大胆管型 ICC:S100 钙结合蛋白(S100calcium binding protein P,S100P)、黏蛋白 5AC(mucin 5AC,MUC5AC)等。③小胆管型 ICC:C-反应蛋白(C-reactiveprotein,CRP)、神经性钙黏蛋白(N-cadherin)、神经细胞相关黏附分子(neural cell adhesion molecule,NCAM/CD56)。④ICC 靶向和免疫治疗相关免疫组化标志物:人类表皮生长因子受体 2(human epidermal growth factor receptor 2,HER2)、错配修复蛋白(MLH1、PMS2、MSH2、MSH6)等。
(3)cHCC-CCA 常用的免疫组化标志物
HCC 和 ICC 两种成分分别表达上述各自肿瘤谱系的标志物。此外,神经上皮干细胞蛋白(nestin)、CD56、CD117 和上皮细胞黏附分子(epithelial cell adhesion molecule,EpCAM)等标志物表达则可能提示肿瘤伴有干细胞分化特征,侵袭性更强、预后更差30。
(4)RNAscope 原位杂交检测标志物
①白蛋白 RNA 原位杂交检测:对判断肝来源的肿瘤有参考价值[120]。②AFP RNA 原位杂交检测:诊断 HCC 的特异性和敏感性优于 AFP 免疫组化[121]。
(5)特殊染色
网状纤维染色:肝板有无增宽、网状纤维支架有无破坏或消失对鉴别肝细胞良性肿瘤和 HCC 有帮助。
- 肝癌分型及靶向/免疫治疗标记物的应用
肝癌分子病理检测的主要目的是:辅助诊断 HCC 特殊亚型;筛选 ICC 常用靶向/免疫治疗药物,指导临床预后监测及个体化治疗,并可以依据分子病理特点对患者进行分层管理(证据等级 2,推荐 B)。
(1)HCC 分型常用的分子病理诊断标志物
①纤维板层型 HCC:具有 DNAJB1-PRKACA 基因融合[103]。②硬化型 HCC:具有结节性硬化症 1/2 基因(tuberoussclerosis 1/2,TSC1/2)突变[103]。③巨梁型 HCC:经常携带TP53 突变和 FGF19 扩增[103]。
(2)ICC 常用分型标志物
①EB 病毒相关的 ICC:推荐采用 EB 病毒编码小核糖核酸(epstein-barr virus encoded ribonucleic acid,EBER)原位杂交检测来检测 EB 病毒感染以筛选免疫检查点抑制剂(immunecheckpoint inhibitors,ICIs)治疗获益人群[122]。②胆管板畸形型 ICC:可出现 ARID1A 突变和缺失表达[123]。
(3)ICC 的靶向/免疫治疗标志物[124]
①大胆管型 ICC:常见成红细胞白血病病毒癌基因同源物2(erythroblastic leukemia viral oncogene homolog 2,ERBB2)基因扩增、v-raf 鼠肉瘤病毒癌基因同源物 B1(v-raf murinesarcoma viral oncogene homolog B1,BRAF)基因突变、Kirsten大鼠肉瘤病毒癌基因同源物(Kirsten ratsarcoma viral oncogenehomolog,KRAS)基因突变、磷脂酰肌醇 4,5-二磷酸 3-激酶催化亚 基α(phosphatidylinositol-4 , 5-bisphosphate 3-kinasecatalytic subunit alpha,PIK3CA)基因突变、神经营养因子受体激酶(neurotrophin receptor kinase,NTRK)基因融合、转染过程中重排(rearranged during transfection,RET)基因融合、微卫星高度不稳定性、高肿瘤突变负荷等[125]。②小胆管型ICC:常见成纤维细胞生长因子受体 2(fibroblast growth factorreceptor 2,FGFR2)基因重排或融合[126]与异柠檬酸脱氢酶 1(isocitrate dehydrogenase 1,IDH1)基因突变[127]。
针对 ICC 的多种治疗靶点,可采用免疫组化、荧光原位杂交、一代测序、二代测序等方法进行检测,还可根据临床需要采用“医疗机构自行研制使用体外诊断试剂”(证据等级 3,推荐 B)。
- 转化/新辅助治疗后肝癌切除标本的病理评估
(1)标本取材
对于临床标注有术前行转化/新辅助治疗的肝癌切除标本,可以按以下流程处理:沿瘤床(肿瘤在治疗前所处的原始位置)最大直径方向切开并测量三维尺寸,详细描述坏死及残存肿瘤范围及占比。直径≤3 cm 的小肝癌应全部取材;而直径>3 cm 的肿瘤应沿最大直径方向按 0.5~1 cm 间隔将肿瘤切开,选择肿瘤坏死及残留最具代表性的切面全部取材,其他切面选择性取材并记录取材的部位和数量等信息。在取材时注意同时留取瘤床及周边肝组织以相互对照,亦可对大体标本照相用于组织学观察的对照。
(2)镜下评估方法
主要评估肝癌切除标本内瘤床的三种成分比例,包括存活肿瘤、坏死区域、肿瘤间质(纤维组织及炎细胞),这三种成分面积之和等于 100%。在评估每张切片上述三种成分百分比的基础上,取均值确定瘤床存活肿瘤的总百分比。
(3)镜下评估指标
①完全病理缓解(complete pathologic response,CPR):是指在术前治疗后,瘤床内未发现存活肿瘤细胞。②明显病理缓解(major pathologic response,MPR):是指在术前治疗后,瘤床内存活肿瘤细胞减少到可以影响临床预后的阈值以下。目前对 HCC 的 MPR 阈值认定尚不一致,如有研究显示,以存活 HCC 细胞≤10%[128]、≤15%[129]、≤30%[130]和≤50%[131]定义MPR 均与预后相关。为此,建议在诊断 MPR 时注明瘤床存活肿瘤细胞的百分比,便于临床根据肿瘤残留情况制定后续治疗方案。
(4)ICIs 联合治疗后肝癌标本的病理评估
对于 ICIs 联合靶向药物或化疗药物治疗后肝癌标本,注意描述淋巴细胞浸润程度及 TLS,同时注意观察癌周肝组织有无免疫相关性肝损伤,包括肝细胞损伤、小叶内炎症及胆管炎等。
- 肝癌病理诊断报告
主要由大体标本描述、免疫组化检查、病理诊断名称和MVI 分级等部分组成,必要时还可以向临床提出说明和建议(附录 7)。此外,还可以酌情开展多结节性/复发性肝癌克隆起源检测、药物靶点检测、生物学行为评估以及预后判断等相关的分子病理学检查,提供临床参考。
要点论述:
(1)肝癌病理诊断主要采用大体标本“7 点”基线取材+显微镜下 MVI 病理分级的一体化诊断模式,为临床提供肝癌术后复发风险、疗效和预后评估的病理依据。
(2)肝癌病理诊断报告内容应规范全面,应特别重视描述影响肝癌预后的重要因素—如肝癌的组织学类型、分化程度、浸润性生长方式、MVI 病理分级和病理分期等。
(3)重视分子病理在肝癌诊断中的应用,辅助诊断 HCC特殊亚型、辅助筛选 ICC 常用靶向/免疫治疗药物。
(4)重视转化/新辅助治疗前肝癌诊断和组织学分型,强调转化/新辅助治疗后切除标本的规范化评估。
(五)肝癌的临床诊断及路线图
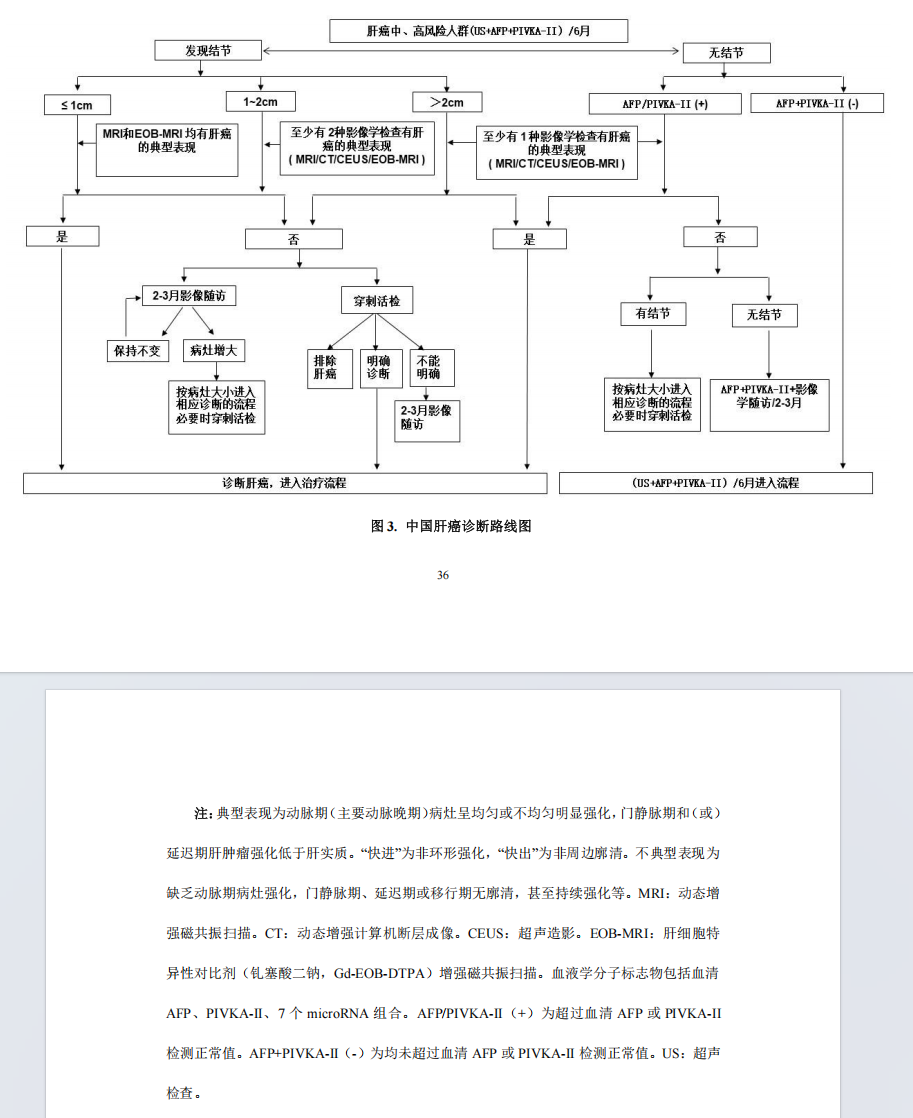
结合肝癌发生的中、高风险因素、影像学特征以及血液学分子标志物,依据路线图的步骤对肝癌进行诊断(图 3)。
(1)肝内 ≤1 cm 结节的诊断路径
肝癌中、高风险人群,至少每隔 6 个月进行 1 次超声检查及血清 AFP、PIVKA-II 检测,发现肝内直径≤1 cm 结节,动态增强 MRI 以及 Gd-EOB-DTPA 增强 MRI 检查同时显示“快进快出”的肝癌典型特征,则可以做出肝癌的临床诊断;若不符合上述要求,可以进行每 2~3 个月的影像学检查随访并结合血清 AFP、PIVKA-II、7 个 microRNA 组合以明确诊断,必要时进行肝病灶穿刺活检。
(2)肝内直径 1~2 cm 结节的诊断路径
肝癌中、高风险人群,随访发现肝内直径 1~2 cm 结节,若动态增强 MRI、动态增强 CT、超声造影或 Gd-EOB-DTPA增强 MRI 四项检查中至少两项检查有典型的肝癌特征,则可以做出肝癌的临床诊断;若上述四项影像学检查无或只有一项典型的肝癌特征,可以进行每 2~3 个月的影像学检查随访并结合血清 AFP、PIVKA-II、7 个 microRNA 组合以明确诊断,必要时进行肝病灶穿刺活检。
(3)肝内直径>2 cm 结节的诊断路径
肝癌中、高风险人群,随访发现肝内直径>2 cm 结节,若动态增强 MRI、动态增强 CT、超声造影或 Gd-EOB-DTPA 增强 MRI 四项检查中至少一项检查有典型的肝癌特征,则可以做出肝癌的临床诊断;若上述四种影像学检查无典型的肝癌特征,可以进行每 2~3 个月的影像学检查随访并结合血清 AFP、PIVKA-II、7 个 microRNA 组合以明确诊断,必要时进行肝病灶穿刺活检。
(4)AFP/PIVKA-II 持续升高的诊断路径
肝癌中、高风险人群,如血清 AFP、PIVKA-II 升高,特别是持续升高,应进行影像学检查以明确肝癌诊断;若动态增强 MRI、动态增强 CT、超声造影或 Gd-EOB-DTPA 增强 MRI四种检查中至少一项检查有典型的肝癌特征,即可以临床诊断为肝癌;如上述四种影像学检查无典型的肝癌特征,在排除妊娠、慢性或活动性肝病、生殖腺胚胎源性肿瘤以及其他消化系统肿瘤的前提下,对于无结节的患者应每隔 2~3 个月进行 1次影像学复查,同时密切随访血清 AFP、PIVKA-II、7 个microRNA 组合变化。
四、分期
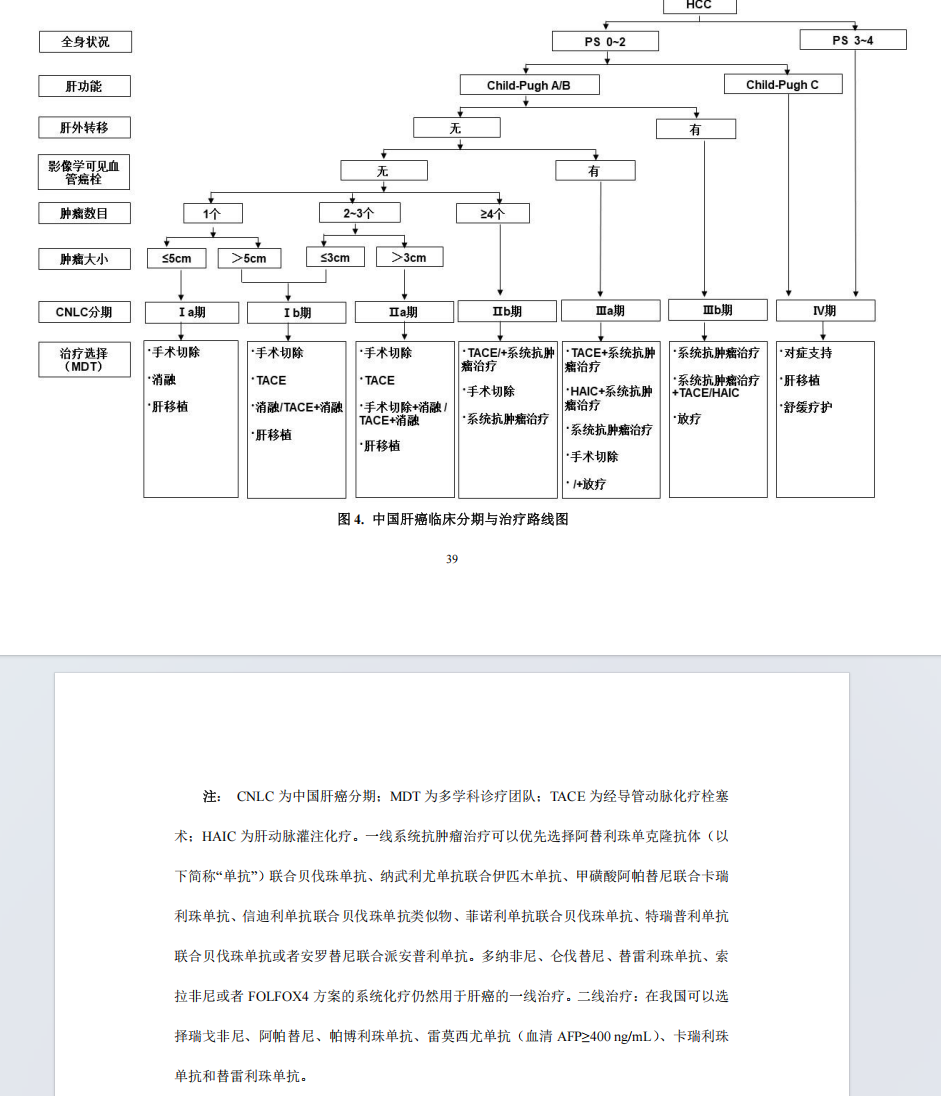
肝癌的分期对于治疗方案的选择、预后评估至关重要。国外有多种分期方案,如:巴塞罗那肝癌临床分期(BarcelonaClinic Liver Cancer,BCLC)、TNM 分期、日本肝病学会(Japanese Society of Hepatology,JSH)分期和亚太肝病研究学会(Asian Pacific Association for the Study of the Liver,APASL)分期等。结合中国的具体国情及实践积累,依据患者体能状态(performance status,PS)、肝肿瘤及肝功能情况,建立中国的肝癌分期方案(China Liver Cancer Staging,CNLC),包括:CNLC Ⅰa 期、Ⅰb 期、Ⅱa 期、Ⅱb 期、Ⅲa 期、Ⅲb 期、Ⅳ期,具体分期方案与治疗路线图见图 4。
CNLC Ⅰa 期:PS 0~2 分,肝功能 Child-Pugh A/B 级,单个肿瘤、直径≤5cm,无影像学可见血管癌栓和肝外转移;
CNLC Ⅰb 期:PS 0~2 分,肝功能 Child-Pugh A/B 级,单个肿瘤、直径>5cm,或 2~3 个肿瘤、最大直径≤3cm,无影像学可见血管癌栓和肝外转移;
CNLC Ⅱa 期:PS 0~2 分,肝功能 Child-Pugh A/B 级,2~3 个肿瘤、最大直径>3cm,无影像学可见血管癌栓和肝外转移;
CNLC Ⅱb 期:PS 0~2 分,肝功能 Child-Pugh A/B 级,肿瘤数目≥4 个,不论肿瘤直径大小,无影像学可见血管癌栓和肝外转移;
CNLC Ⅲa 期:PS 0~2 分,肝功能 Child-Pugh A/B 级,不论肿瘤直径大小和数目,有影像学可见血管癌栓而无肝外转移;
CNLC Ⅲb 期:PS 0~2 分,肝功能 Child-Pugh A/B 级,不论肿瘤直径大小和数目,不论有无影像学可见血管癌栓,但有肝外转移;
CNLC Ⅳ期:PS 3~4 分,或肝功能 Child-Pugh C 级,不论肿瘤直径大小和数目,不论有无影像学可见血管癌栓,不论有无肝外转移。
五、治疗
肝癌治疗具有 MDT 和多种治疗方法并存的特点。常见的治疗方法包括肝切除术、肝移植术、消融治疗、经动脉介入治疗、放射治疗、系统性抗肿瘤治疗、中医药等手段。每种治疗手段均存在其特有的优势和局限性,且适应证互有重叠。因此,规范而精准的治疗决策应基于权威指南及高级别循证医学证据,并结合各领域的最新进展与研究成果。然而,单一学科对其他领域治疗方法的知识更新可能存在滞后性,这进一步凸显了 MDT 在肝癌诊疗中的重要性[132]。通过 MDT的沟通与协作,能够为患者制定最适宜的个体化治疗方案,延长患者 OS 并最大限度地提高患者的生存质量。目前肝癌MDT 的重要性与必要性已成为业界广泛共识,然而受实际条件的影响,不同地区和不同单位之间肝癌 MDT 的实施方式和水平仍存在较大差异。建议各级医院将 MDT 管理纳入医疗质量管理体系,由医疗行政主管部门与指定的 MDT 负责人共同监督,以固定时间、固定地点、固定人员的形式开展MDT 会诊。对于基层医院,若因资源限制难以独立组织MDT,可通过“医联体”或“远程医疗”等方式实现协作。随着国家癌症中心《中国肝癌规范诊疗质量控制指标(2022 版)》的发布与实施,全国肝癌诊疗的规范化与同质化水平有望进一步提升。
(一)外科治疗
外科治疗是肝癌获得长期生存的重要手段,主要包括肝切除术和肝移植术。
- 肝癌的手术切除
(1)肝癌手术切除的基本原则
①根治性:完整切除肿瘤及可能侵犯的组织,切缘无肿瘤残留;②安全性:保留足够体积且有功能的肝组织(具有良好的血供以及血液、胆汁回流)以确保术后肝功能代偿。实现“病灶清除、肝脏保护和损伤控制”三者的最佳平衡。
(2)手术安全性的评估及术后随访在术前应对患者的全身情况、肝脏储备功能及肝脏肿瘤情况(分期及位置)进行全面评估:常采用美国东部肿瘤协作组提出的功能状态评分(Eastern Cooperative OncologyGroup performance status,ECOG PS)评估患者的全身情况,使用 NRS-2002 评分表作为营养筛查工具;采用肝功能Child-Pugh 评分、白蛋白-胆红素(albumin bilirubin,ALBI)评分、吲哚菁绿(indocyanine,ICG)清除试验、剪切波弹性测定肝脏硬度或终末期肝病模型(model for end-stage liverdisease,MELD)评分,评估肝脏储备功能情况。人工智能辅助的术前规划,如深度学习模型可以有助于预测术后肝功能衰竭发生的风险[133-136](证据等级 3,推荐 C)。精确地评估门静脉高压的程度(如利用肝静脉压力梯度测定等42)[137-138],有助于筛选适合手术切除的患者[139-140(] 证据等级 3,推荐 B)。如预期保留肝脏组织体积较小,则可以采用 CT/MRI测定剩余肝脏体积(future liver remnant,FLR),并计算 FLR占标准肝脏体积(standard liver volume,SLV)的百分比。通常认为,肝功能 Child-Pugh A 级、ICG 15 min 潴留率(ICG-R15)<30%是安全实施手术切除的必要条件;FLR 占SLV 的 40%以上(伴有慢性肝病、肝实质损伤或肝硬化者)或 30%以上(无肝纤维化或肝硬化者)是安全实施手术切除的重要条件。术中对预留肝脏检测 ICG-R15 是预测肝癌切除术后(尤其是大范围肝切除术后)肝功能衰竭的重要指标,有助于术中决策的制定[141-142]。加速康复外科(enhancedrecovery after surgery,ERAS)[143]的实施进一步促进了患者术后的快速康复。
肝癌患者术后 1~2 个月需复诊 1 次,之后每隔 3 个月密切监测影像学(超声检查,必要时选择动态增强 CT、动态增强 MRI、CEUS 或 Gd-EOB-DTPA 增强 MRI)及血清 AFP、PIVKA-II 和 7 个 microRNA 组合等肿瘤学标志物的改变,2年后随访时间可适当延长至 3~6 个月,持续时间建议终身随访(证据等级 3,推荐 B)。
(3)肝癌手术切除的适应证
①肝脏储备功能良好的 CNLC Ⅰa~Ⅱa 期肝癌的首选治疗方式是手术切除。既往研究结果显示:对于直径≤3 cm 肝癌,手术切除的 OS 率类似或稍优于消融治疗[144-146](证据等级 1,推荐 A),但手术切除后局部复发率显著低于消融治疗[147-151]。对于复发性肝癌,手术切除的预后仍然优于射频消融(radiofrequency ablation,RFA)[152(] 证据等级 2,推荐 B)。对于 2~3 枚结节的肝癌,手术切除的预后优于消融治疗和TACE [153-154](证据等级 2,推荐 B)。②对于 CNLC Ⅱb 期肝癌,多数情况下不宜首选手术切除,而以 TACE/+系统抗肿瘤为主的非手术治疗为首选。如果肿瘤局限在同一肝段或半肝者,或可以同时行术中消融处理切除范围外的病灶;即使肿瘤数目>3 个,经过 MDT 讨论,手术切除有可能获得比其他治疗更好的效果[155-158],也可以选择手术切除(证据等级 2,推荐 B)。③对于 CNLC Ⅲa 期肝癌,绝大多数情况下不宜首选手术切除,尤其是合并门静脉主干癌栓者,而以 TACE/肝动脉灌注化疗(hepatic arterial infusion chemotherapy,HAIC)+系统抗肿瘤治疗为主的非手术治疗为首选。但有研究提示,肝切除术治疗晚期非转移性肝癌的 OS 和无进展生存时间(progression free survival,PFS)显著优于索拉非尼方案[159]。手术切除治疗 CNLC Ⅲa 期肝癌的数据大部分来源于亚洲国家[160-161],少部分来自西方国家[162-163]。如符合以下情况,经过 MDT 讨论,也可考虑行手术切除:合并门静脉分支癌栓(程氏分型Ⅰ/Ⅱ型)者,若肿瘤局限于半肝或肝脏同侧,可以考虑手术切除肿瘤同时完整切除癌栓,术后再实施 TACE治疗、门静脉化疗或其他系统抗肿瘤治疗[164-165],以延长生存(证据等级 3,推荐 C);此类患者术前接受三维适形放射治疗,亦可以改善术后生存[166](证据等级 2,推荐 B);合并胆管癌栓但肝内病灶可同时切除者;部分肝静脉受侵犯但肝内病灶可以切除者。门静脉主干癌栓(程氏分型Ⅲ型)者术后短期复发率高,多数患者的术后生存不理想,因此不建议直接行手术切除[167](证据等级 3,推荐 B)。④对于伴有肝门部淋巴结转移肝癌(CNLC Ⅲb 期),经过 MDT 讨论,可以考虑完整切除肿瘤的同时行肝门淋巴结清扫或术后外放射治疗。周围脏器受侵犯可以一并切除者,也可以考虑手术切除。⑤此外,对于术中探查发现不适宜手术切除肝癌,可以考虑行术中其他的局部治疗措施(如消融治疗),或待手术创伤恢复后接受后续抗肿瘤治疗。
(4)肝癌根治性手术切除的判断标准
①术中判断标准:肝静脉、门静脉、胆管以及下腔静脉未见肉眼癌栓;无邻近脏器侵犯,无肝门淋巴结或远处转移;切除的肝断面组织学检查无肿瘤细胞残留,即手术切缘阴性。②术后判断标准:术后 1~2 个月行超声、CT 或 MRI 检查(必须有其中 2 项)未发现肿瘤病灶残留;如术前血清 AFP、PIVKA-II 或 7 个 microRNA 组合等肿瘤标志物升高者,则要求术后 2~3 个月肿瘤标志物水平降至正常范围内。术后肿瘤标志物如 AFP 下降速度,可以早期预测手术切除的彻底性[168]。
(5)常用的肝癌手术切除技术
精准肝切除技术主要包括入肝和出肝血流控制技术、肝脏离断技术以及止血技术。人工智能的术前三维重建,实现个体化肝脏体积计算和虚拟肝切除,有助于在实现肿瘤根治性切除的前提下,设计更为精准的切除范围和路径以保护剩余肝脏的管道、保留足够 FLR[169-176](证据等级 2,推荐 A)。术中超声检查及 CEUS、术中荧光染色或人工智能增强影像融合技术可以有助于发现微小病灶、标记切除范围和获得肿瘤阴性切缘[177](证据等级 3,推荐 B)。术中导航系统利用增强现实技术和混合现实技术与人工智能的融合,提高了手术的安全性。
近年来,微创手术(包括腹腔镜肝切除术和机器人辅助肝切除术)飞速发展。腹腔镜肝切除术具有创伤小和术后恢复快等优点[178-179](证据等级 1,推荐 A)。早期肝癌接受腹腔镜肝切除术与开腹手术的 5 年 OS 率相当[180(] 证据等级 2,推荐 B)。对于肿瘤直径≤5 cm、位于外周肝段(CouinaudⅡ~Ⅵ段)的肝癌可优先选择腹腔镜肝切除;肿瘤直径<5 cm但位于困难部位,肿瘤直径 5~10 cm 以及符合米兰标准的多发肝癌可在有经验的医疗中心实施;对于巨大肝癌、多发肝癌、位于困难部位及中央区紧邻重要管道、合并门静脉癌栓(程氏分型Ⅰ/Ⅱ型)的肝癌和肝癌合并重度肝硬化者,建议经严格选择后由经验丰富的医师实施[179]。对于合并门静脉肉眼癌栓、肿瘤破裂出血的肝癌患者,不建议行腹腔镜肝切除术。腹腔镜手术中如果发现肝癌破裂应及时中转开腹手术。机器人辅助肝切除术与腹腔镜肝切除术相比较,其手术并发症发生率更低、累积生存率相似,但成本效益比仍需进一步优化[180-182](证据等级 2,推荐 B)。
解剖性肝切除与非解剖性肝切除均为常用的肝切除技术,都需要保证有足够的切缘才能获得良好的肿瘤学效果。解剖性肝切除相对于非解剖性肝切除,尤其对于伴有 MVI的肝癌病例,虽然 OS 没有区别,但术后并发症发生率及局部复发率更低[183-185](证据等级 2,推荐 B)。有研究发现,宽切缘(≥1 cm 的切缘)的肝切除效果优于窄切缘的肝切除术[186-187](证据等级 2,推荐 B),特别是对于术前预判存在MVI 的患者[188]。对于巨大肝癌,可以采用前入路肝切除术[189]。对于多发性肝癌,可以采用手术切除结合术中消融治疗[190](证据等级 3,推荐 C)。
- 以手术切除为目标的综合治疗策略
基于既往的大宗病例的数据,CNLC Ⅱb、Ⅲa、Ⅲb 肝癌手术后总体生存虽然不令人满意,但当前系统抗肿瘤治疗与综合治疗取得长足进步,局部治疗和(或)系统抗肿瘤治疗控制肿瘤的效果可以为中晚期肝癌患者提高手术切除率、降低术后复发转移和改善预后提供更多可能[191-192],手术适应证的适度扩大成为共识。探索中晚期肝癌以手术切除为目标的综合治疗新策略已成为近期关注重点,最终以延长肝癌患者生存为主要目的。
(1)不可切除肝癌的转化治疗
转化治疗指不适合手术切除的肝癌,经过干预后获得根治性手术切除的机会,干预手段包括有功能的 FLR 转化、肿瘤学转化等。手术切除是转化成功后患者获得长期生存的重要手段[193]。近期,TALENTOP 研究通过前瞻随机对照临床研究证实,接受阿替利珠单克隆抗体(以下简称“单抗”)联合贝伐珠单抗治疗转化成功后的患者,接受手术切除并序贯维持治疗 12 个月,至治疗失败时间由持续系统治疗组的 11.8个月延长至 20.4 个月(HR=0.60,P=0.015),并显示出 OS改善的趋势,整体安全性可控(证据等级 1,推荐 A)。
在肝癌转化治疗中,有功能的 FLR 转化是重要组成部分。FLR 不足是肝癌外科学无法手术切除的重要原因。对于这类患者,转化治疗的目标就是由 FLR 不足转变为有功能的FLR 足够[194]。
门静脉栓塞术(portal vein embolization,PVE)通过栓塞肿瘤所在半肝的门静脉分支,促使 FLR 代偿性增生后再行肿瘤切除。合理选择患者的情况下,PVE 的转化成功率可60%~80%,并发症发生率约为 10%~20%。然而,PVE 术后FLR 增生所需时间相对较长,通常需要 4~6 周,约 20%以上患者在等待期间因肿瘤进展或 FLR 增生不足而最终失去手术机会[195-196](证据等级 3,推荐 B)。针对这部分患者,目前可采取联合 TACE [197]、肿瘤引流区域肝静脉栓塞[198]、患侧肝动脉结扎[199]等策略,以进一步促进 FLR 增生并控制肿瘤进展,或采用拯救性联合肝脏分隔和门静脉结扎的二步肝切除术(associating liver partition and portal vein ligation forstaged hepatectomy,ALPPS)完成肿瘤切除[200]。PVE 的禁忌证包括门静脉主干或一级分支癌栓、肿瘤广泛转移、严重门静脉高压及明显凝血功能障碍。对于预期有功能的 FLR 增生时间较长(例如较严重肝硬化、年龄较大的患者),肿瘤进展可能较快的患者需要谨慎使用。
ALPPS 作为近期肝脏外科的主要创新技术,ALPPS 通常可在约 1~2 周诱导产生 47%~192%的 FLR 增生率,远远高于 PVE。因两期手术间隔时间短,故能最大程度减少肿瘤进展风险,肿瘤切除率达 95%~100%[201-202]。随着手术技术的进步和经验的积累,与 ALPPS 相关的手术并发症及死亡率已较 ALPPS 开展初期减少。近年来出现多种 ALPPS 改进术式,主要集中于一期手术肝断面分隔操作[部分分隔和使用RFA、微波消融(microwave ablation,MWA)、止血带等方式分隔]以及采用腹腔镜微创入路行 ALPPS,进一步提高了ALPPS 手术的安全性。若 ALPPS 一期术后 2 周,有功能的FLR 仍不足以达到手术切除要求,则可以行动脉栓塞(transarterial embolization,TAE),此术式被称为 TAE 挽救性 ALPPS(TAE-salvaged ALPPS),其 1 周后几乎达到 100%的二期手术切除率[203]。有 RCT 研究已经证实,ALPPS 较 PVE在快速诱导 FLR 增生的能力方面具有显著优势[204](证据等级 2,推荐 A)。与转化治疗中的肿瘤学转化相比,在手术切除成功率、间隔时间方面,通过研究数据的对比,ALPPS 具有显著的优势,但其最终的适用人群、远期疗效等还需更多后续的研究支持。当然,ALPPS 也可与肿瘤学转化序贯、联合应用,进一步提高转化成功率[205]。ALPPS 一般应限定于以下患者:年龄≤70 岁、肝功能正常(Child‑Pugh A 级,ICG-R15<20%)、FLR 不足(正常肝脏者,FLR/SLV<30%;伴有慢性肝病和肝损伤者,FLR/SLV<40%)、一般状态良好、手术耐受力良好、无严重肝硬化、无严重脂肪肝、无严重门静脉高压症者。
肿瘤学转化是肝癌转化治疗的另一重要途径。局部治疗手段包括 TACE [206]、HAIC[207]、放疗等局部治疗手段为初始不可切除肝癌创造手术切除机会,并且能够转化为生存获益(证据等级 3,推荐 B)。TACE 或 HAIC 与系统抗肿瘤治疗的联合可进一步提高转化率[208-211]。对于肿瘤负荷较大或合并门脉癌栓(尤其是主干癌栓),暂时不能接受外科手术治疗的肝癌,多项临床研究显示 HAIC 治疗具有较高的客观缓解率(objective response rate,ORR),部分患者经 HAIC 治疗后肿瘤体积缩小或门脉癌栓退缩,提高了转化治疗的成功率(证据等级 3,推荐 B)。HAIC 联合 TACE [212]、放疗[213]、靶向药物和(或)免疫治疗可以进一步提高转化的成功率。
系统抗肿瘤治疗在肿瘤学转化中同样具有重要作用。抗血管生成药物联合免疫治疗、靶向药物已成为不可切除或中晚期肝癌的重要治疗方式,是实现肝癌转化手术的重要手50段[214-215]。TALENTOP 研究显示阿替利珠单抗联合贝伐珠单抗治疗后转化成功患者,相比持续系统治疗,接受肝切除术序贯阿替利珠单抗联合贝伐珠单抗维持治疗 12 个月,可带来具有临床意义的 PFS 提升并呈现 OS 获益的趋势(证据等级1,推荐 A)。单从系统抗肿瘤治疗方案选择的角度,需要鉴别无法行根治切除的原因、重视病因学的处理、在 MDT 框架下严格随访肿瘤缓解的持续时间和缓解深度,严密监测系统抗肿瘤治疗的毒性及对转化治疗手段的可能影响,积极探索转化治疗前后肿瘤免疫微环境的变化,积极开展高级别循证医学证据的大型临床研究,力争使患者最大程度获益。
(2)肝癌的新辅助治疗
新辅助治疗是指对于适合手术切除但具有术后中、高危复发转移风险的肝癌,在术前先进行局部治疗和(或)系统抗肿瘤治疗,以期消灭微小病灶、降低术后复发与转移、延长生存期。术前评估的中、高危复发转移因素包括:血管侵犯、单发肿瘤直径>5 cm、多发肿瘤、邻近脏器受累、术前AFP 水平较高等。随着靶向药物、ICIs 等新药的快速发展以及肝癌局部治疗技术的不断改进,新辅助治疗在肝癌中的应用取得了初步进展[130,216-217]。
近期 CARES-009 研究证实,对于适合手术切除但具有术后中、高危复发风险的肝癌患者,卡瑞利珠单抗联合甲磺酸阿帕替尼在新辅助及术后辅助的序贯使用,能显著提高患者的无事件生存期(42.1 个月 vs. 19.4 个月,HR=059,P=0.004),同时安全性可控[131](证据等级 1,推荐 A)。
新辅助治疗也存在风险,应严格选择适宜人群,同时根据新辅助治疗的目标选择适宜的治疗方案。
(3)肝癌术后辅助治疗
肝 癌 切 除 术 后 5 年 肿 瘤 复 发 转 移 率 高 达50%~88%[218-219]。术后 4~8 周实施的辅助治疗是降低肿瘤复发转移风险,改善患者生存的重要手段。相比于新辅助治疗,术后辅助治疗可以根据术后病理及分子分型更进一步精准选择治疗人群及个体化治疗方案,且不会因此而延期手术。术后辅助治疗的人群主要是适合中、晚期肝癌经新辅助/转化后手术以及术后病理明确为中、高危复发者。虽然不同研究定义的术后中、高危复发转移因素不同,但术后评估的中、高危复发转移因素一般包括:肿瘤破裂、肿瘤直径>5 cm、多发肿瘤、MVI、大血管侵犯、淋巴结转移、窄切缘、组织分化 Edmondson-Steiner Ⅲ~Ⅳ级等[220-222]。新的分子水平标志物(如 ctDNA、微小残留病灶[223])可为患者术后复发转移风险分层提供新的依据。精准筛选辅助治疗的获益人群仍是目前亟待解决的难题。
对于具有术后中、高危复发转移风险的患者,目前尚无标准的辅助治疗方案。虽有争议[224],但多项随机对照研究已证实术后辅助 TACE 治疗可以有效减少复发转移,延长生52存[225-227](证据等级 1,推荐 A)。有研究发现,肝癌大体病理形态分型具有指导术后辅助 TACE 治疗选择的价值,其中浸润型患者需优先考虑术后辅助 TACE,可显著延长生存期[228]。 采 用 5- 氟 尿 嘧 啶 ( 5-FU ) / 奥 沙 利 铂 / 亚 叶 酸 钙(mFOLFOX)方案的 HAIC 可以降低合并 MVI 的肝癌患者复发转移率[229](证据等级 2,推荐 B)。对于手术切除、RFA或无水乙醇注射治疗(percutaneous ethanol injection,PEI)的肝癌患者,活化的杀伤细胞治疗亦可显著延长无复发生存时间(recurrence free survival,RFS)和 OS [230](证据等级 2,推荐 B);免疫调节剂(如胸腺法新[231])也具有类似作用。另一项前瞻性多中心随机对照Ⅲ期临床研究[232]证明,中药槐耳颗粒可以延长术后的 RFS(证据等级 1,推荐 A)。另外,对于 HBV 感染的肝癌患者,核苷类似物抗病毒治疗有助于降低根治性切除术后的复发转移,应长期服用[233](证据等级1,推荐 A)。对于病毒性肝炎相关肝癌患者,术后辅助使用聚乙二醇化干扰素,可以提高 OS 及 RFS,并且不会带来严重的不良反应[234](证据等级 2,推荐 B)。对于 HCV 感染的肝癌患者,直接抗病毒药物(DAAs)以获得持续的病毒学应答,目前没有确凿的数据表明直接抗病毒药物治疗与肝癌术后肿瘤复发转移风险增加或降低、复发时间或术后生存时间的差异相关[235]。此外,对于伴有门静脉癌栓患者术后经门静脉置管化疗联合 TACE,也可以延长患者生存期[165](证据等级 3,推荐 B)。近年来,系统抗肿瘤治疗在肝癌辅助治疗中的研究也在不断深入[236],多项在晚期肝癌中有效的治疗方案正在积极探索在辅助治疗中的价值。IMbrave050 最新数据表明,与主动监测相比,阿替利珠单抗联合贝伐珠单抗方案的 PFS 优势未随时间持续(HR=0.90,95% CI=0.72~1.12),且 OS 时间无改善趋势[237]。
目前,辅助治疗的应用仍存在诸多争议,包括适用人群的界定(适应证)、最佳治疗方案的选择以及治疗持续时间的确定等。
要点论述:
(1)肝切除术是肝癌患者获得长期生存的重要手段。
(2)在术前应对患者的全身情况、肝脏储备功能及肝脏肿瘤情况(分期及位置)进行全面评估。
(3)肝脏储备功能良好的 CNLC Ⅰa~Ⅱa 期肝癌的首选治疗是手术切除。CNLC Ⅱb、Ⅲa 期肝癌,经 MDT 评估,部分患者仍有机会从手术切除中获益。
(4)腹腔镜技术具有创伤小和术后恢复快等优点,优先选择肿瘤直径≤5 cm、病灶位于外周肝段(Couinaud Ⅱ~Ⅵ段)的肝癌实施。
(5)肝癌术后 1~2 个月患者需复诊 1 次,之后每隔 3个月密切监测影像学及 AFP、PIVKA-II 和 7 个 microRNA 组合等肿瘤学标志物的改变,2 年之后可适当延长至 3~6 个月,持续时间建议终身随访。
(6)转化治疗指不适合手术切除的肝癌,经过干预后获得根治性手术切除的机会,干预手段包括有功能的 FLR 转化、肿瘤学转化等。
(7)新辅助治疗是指对于适合手术切除但具有术后中、高危复发转移风险的肝癌,在术前先进行局部治疗或系统抗肿瘤治疗,以期消灭微小病灶,降低术后复发率、延长生存期;但新辅助治疗也存在风险,应严格选择适宜人群,同时根据新辅助治疗的目标选择适宜的治疗方案。
(8)对于中、晚期肝癌经新辅助/转化后手术以及术后病理明确为中、高危复发的肝癌,目前尚无标准的辅助治疗方案,术后可以尝试采取抗病毒、TACE、HAIC 等辅助治疗以降低术后复发转移率,延长生存。
- 肝脏移植
(1)肝癌肝移植适应证
肝移植是肝癌根治性治疗手段之一,尤其适用于肝功能失代偿、不适合手术切除及消融治疗的早期肝癌(证据等级2,推荐 A)。合适的肝癌肝移植适应证是提高肝癌肝移植疗效、确保宝贵的供肝资源得到公平合理应用、平衡有(或)无肿瘤患者预后差异的关键[238](证据等级 3,推荐 B)。
关于肝癌肝移植适应证,国际上主要采用米兰(Milan)标准、美国加州大学旧金山分校(University of California atSan Francisco,UCSF)标准、美国器官共享联合网络(UnitedNetwork for Organ Sharing,UNOS)标准等。国内尚无统一标准,已有多家单位和学者陆续提出了不同的标准,包括上海复旦标准[239]、杭州标准[240]、华西标准[241]和三亚共识[242]等。上述国内标准在未明显降低术后 OS 率的前提下,均不同程度地扩大了肝癌肝移植的适用范围,使更多的肝癌患者因肝移植手术而受益,但是需要多中心协作研究以支持和证明,从而获得高级别的循证医学证据。经专家组充分讨论,现阶段本指南推荐采用 UCSF 标准,即单个肿瘤直径≤6.5cm;肿瘤数目≤3 个,其中最大肿瘤直径≤4.5 cm,且肿瘤直径总和≤8.0 cm;无大血管侵犯。结合 AFP、AFP-L3 和PIVKA-II 等肝癌生物标志物,有助于进一步指导肝癌肝移植受者的危险分层及筛选[243-245]。中国人体器官分配与共享基本原则和核心政策对肝癌肝移植有特别说明,规定肝癌受体可以申请早期肝癌特例评分,申请成功者可以获得 MELD 评分 22 分(≥12 岁肝脏移植等待者),每 3 个月进行肝癌特例评分续期。
符合肝癌肝移植适应证的肝癌患者在等待供肝期间可以接受桥接治疗控制肿瘤进展,以防止患者失去肝移植机会,是否降低肝移植术后复发转移概率目前证据有限[246-247](证据等级 2,推荐 C)。桥接治疗的方式目前主要是局部治疗,包括 TACE、选择性内放射治疗(selective internal radiationtherapy,SIRT)、消融治疗、立体定向放射治疗(stereotacticradiotherapy,SBRT)等。
部分肿瘤负荷超出肝移植适应证标准的肝癌患者可以通过降期治疗将肿瘤负荷缩小而符合适应证范围。降期治疗成功后的肝癌患者,肝移植术后疗效预后优于非肝移植患者[248-249](证据等级 2,推荐 B)。最近的多中心前瞻性研究进一步证实肝癌肝移植术前肿瘤降期的可行性以及降期后对生存的益处[250-251]。降期治疗这个过程也可以作为一种选择工具来识别具有有利的肿瘤生物学特性的肝移植受者。降期治疗引起肝功能失代偿的风险必须重视。
ICIs 在肝癌肝移植受者术前降期和(或)桥接治疗中的应用,是否会增加术后排斥和移植物损失的风险,有待进一步观察[252]。
鉴于目前肝源日益短缺,采用扩大标准供体范围(通常可包括年龄较大、肝脏脂肪变性以及/或携带可传播感染的供体)、活体供肝肝移植(包括废弃供肝肝移植[253])、劈离式肝移植以及机器灌注技术,可能会扩大供肝来源。
(2)肝癌肝移植术后复发转移的预防和治疗肿瘤复发转移是肝癌肝移植术后面临的主要问题[254]。其危险因素包括肿瘤分期、肿瘤血管侵犯、术前血清 AFP 水平以及免疫抑制剂用药方案等。RETREAT(Risk Estimation ofTumor Recurrence After Transplant)评分[255]及其改进模型[256]有助于肝移植后复发风险预测。术后早期撤除或无激素方案[257]、减少肝移植后早期钙调磷酸酶抑制剂的用量可以降低肿瘤复发转移率[258](证据等级 3,推荐 C)。对于术前 AFP 升高或根据诸如 RETREAT 等风险评分处于肝移植术后高复发风险的患者,基于哺乳动物雷帕霉素靶蛋白(mTOR)的免疫抑制治疗可能有益[259](证据等级 2,推荐 C)。
肝癌肝移植术后最常见的复发转移部位是肺(约 40%)及肝脏(33%)。肝癌肝移植术后一旦肿瘤复发转移(75%的病例发生在肝移植术后 2 年内),病情进展迅速,复发转移后患者的中位生存时间大约为 1 年[260-261]。在 MDT 的基础上,采取包括变更免疫抑制方案、再次手术切除、TACE、消融治疗、放射治疗、系统抗肿瘤治疗等综合治疗手段,可能延长患者生存时间[262-263](证据等级 3,推荐 B)。移植术后的密切监测、接受潜在的根治性治疗与改善复发转移后生存有关[264]。ICIs 用于肝癌肝移植的辅助治疗或术后复发的治疗仍需慎重[265-266](证据等级 3,推荐 C),必须在抑制同种异体移植物排斥反应和重新激活肿瘤免疫反应之间取得平衡。
要点论述:
(1)肝移植是肝癌根治性治疗手段之一,尤其适用于肝功能失代偿、不适合手术切除及消融治疗的早期肝癌。
(2)推荐 UCSF 标准作为中国肝癌肝移植适应证标准。
(3)局部治疗在肝癌肝移植的降期治疗或桥接治疗中具有重要作用。
(4)肝癌肝移植术后一旦肿瘤复发转移,病情进展迅速,在 MDT 基础上的综合治疗,可以延长患者生存时间。
(二)消融治疗
目前消融治疗已经被认为是手术切除之外治疗小肝癌的根治性治疗方式,消融治疗具有对肝功能影响少、创伤小、疗效确切的特点,在一些早期肝癌患者中可以获得与手术切除相类似的疗效。
肝癌消融治疗是借助医学影像技术的引导,对肿瘤病灶靶向定位,局部采用物理或化学的方法直接杀灭肿瘤组织的一类治疗手段。主要包括RFA、MWA、冷冻消融(cryoablation,CRA)、高强度超声聚焦消融(high intensity focused ultrasoundablation,HIFU)、激光消融(laser ablation,LA)、不可逆电穿孔(irreversible electroporation,IRE)、PEI 等。消融治疗常用的引导方式包括超声、CT 和 MRI,其中最常用的是超声引导,具有方便、实时、高效的特点。CT、MRI 可以用于观察和引导常规超声无法探及的病灶以及消融方案规划。
消融的路径有经皮、腹腔镜或开腹三种方式。大多数的小肝癌可以经皮穿刺消融,具有经济、方便、微创等优点。影像学引导困难的肝癌或经皮消融高危部位的肝癌(如贴近心脏、膈肌、胃肠道、胆囊等),可以考虑采用经腹腔镜消融、开腹消融或水隔离技术辅助经皮消融的方法,并可使用多模影像融合导航技术引导穿刺。
消融治疗主要适用于 CNLC Ⅰa 期及部分Ⅰb 期肝癌(即单个肿瘤、直径≤5 cm;或 2~3 个肿瘤、最大直径≤3 cm);无血管、胆管和邻近器官侵犯以及远处转移,肝功能Child-Pugh A/B 级者,可以获得根治性的治疗效果[267-271](证据等级 1,推荐 A)。对于不适合单纯手术切除的直径 3~7 cm的单发肿瘤或多发肿瘤,可以采用消融联合手术切除或TACE 治疗[272-276](证据等级 2,推荐 B)
- 目前常用消融治疗手段
(1)RFA:RFA 是肝癌微创治疗常用消融方式,其优点是操作方便、住院时间短、疗效确切、消融范围可控性好,特别适用于高龄、合并其他疾病、严重肝硬化、肿瘤位于肝脏深部或中央型肝癌的患者。对于早期肝癌,RFA 的 OS 类似或略低于手术切除,但并发症发生率低、住院时间较短[267,269-271,277](证据等级 1,推荐 A)。对于单个直径≤2 cm 肝癌,有证据显示 RFA 的疗效与手术切除类似,特别是位于中央型的肝癌[278-279](证据等级 2,推荐 A)。RFA 治疗的技术要求是肿瘤整体灭活和具有足够的消融安全边界,并尽量减少正常肝组织损伤,其前提是对肿瘤浸润范围的准确评估和卫星灶的识别。因此,强调精准消融,治疗前运用多模态影像学检查和治疗前后影像学配准评估。超声造影技术有助于确认肿瘤的实际大小和形态、界定肿瘤浸润范围、检出微小肝癌和卫星灶,尤其在体内如有金属物或起搏器植入时评估病灶,或超声引导消融过程中为制定消融方案、完全灭活肿瘤提供可靠的参考依据。
(2)MWA:近年来 MWA 应用比较广泛,在局部疗效、并发症发生率以及远期生存方面与 RFA 相比都无显著差异[280-284](证据等级 1,推荐 A)。其特点是消融效率高、所需消融时间短、能降低 RFA 所存在的“热沉效应”,尤其对于邻近血管的肿瘤、富血供肿瘤和较大肿瘤具有更彻底的消融毁损效果。利用温度监控系统有助于调控功率、时间等参数,确定有效热场范围,保护热场周边组织避免热损伤,提高MWA 消融安全性。至于 MWA 和 RFA 这两种消融方式的选择,可以根据肿瘤的大小、位置,选择更适宜的消融方式。
(3)CRA:CRA 治疗途径与 RFA 和 MWA 相同,可经皮、经腹腔镜或开腹直视下完成,但需注意患者凝血功能。CRA 治疗≤2 cm 肝癌效果与 MWA、RFA 治疗手段相似[285](证据等级 2,推荐 B)。
(4)IRE:为非热消融,具有不产生热损伤、不受热沉效应影响等优势。对邻近重要组织如胆管、肠管等损伤小,特别适用于治疗邻近血管、胆管、膈肌、胃肠道或肝门等危险部位的肿瘤[286-287](证据等级 2,推荐 B)。但 IRE 对于麻醉要求较高,常需静脉麻醉结合肌松剂;且 IRE 的多针平行操作技术要求较高。
(5)PEI:PEI 对直径≤2 cm 的肝癌消融效果确切,远期疗效与 RFA 类似,但>2 cm 肿瘤局部复发率高于 RFA[288](证据等级 2,推荐 B)。PEI 的优点是安全,特别适用于癌灶贴近肝门、胆囊及胃肠道组织等高危部位,但需要多次、多点穿刺以实现药物在瘤内弥散作用,因而目前多用于热消融技术的辅助治疗。
- 基本技术要求
操作医师必须经过严格培训和积累足够的实践经验,掌握各种消融技术手段的优缺点与治疗选择适应证、禁忌证。治疗前应该全面充分地评估患者的全身状况、肝功能状态、凝血功能及肿瘤的大小、位置、数目以及与邻近器官的关系,制定合理的穿刺路径、消融计划及术后维护,在确保安全的前提下,达到有效的消融安全范围。
根据肿瘤的大小、位置,强调选择适合的影像引导设备(超声或 MRI/CT 等)和消融方法(RFA、MWA、CRA 或PEI 等),单一影像显示欠清的可采用多模态融合影像引导。
邻近肝门部或靠近一、二级胆管的肝癌需要谨慎应用消融治疗,避免发生损伤胆管等并发症。采用 PEI 的方法较为安全,或消融联合 PEI。如果采用热消融方法,肿瘤与一、二级肝管之间要有足够的安全距离(至少超过 5 mm),或者采用水隔离等辅助技术保护肝管,并采用安全的消融参数(低功率、短时间、间断辐射)。对于有条件的消融设备推荐使用温度监测方法。
消融范围应力求覆盖包括至少 5 mm 的癌旁组织,以获得“安全边缘”,彻底杀灭肿瘤。对于边界不清晰、形状不规则的癌灶,在邻近肝组织及结构条件许可的情况下,建议适当扩大消融范围。
- 对于直径 3~5cm 的肝癌治疗选择
多项前瞻性随机对照临床试验和系统回顾性分析显示,直径 3~5 cm 的肿瘤宜首选手术切除[270,289](证据等级 1,推荐 A)。在临床实践中,应该根据患者的一般状况和肝功能,肿瘤的大小、数目、位置决定,并结合从事消融治疗医师的技术和经验,全面考虑后选择合适的初始治疗手段。通常认为,如果患者能够耐受肝切除术,尤其是肝癌位置表浅、位于肝脏边缘或不适合消融的高危部位肝癌,均应首选手术切除。对于直径 3~5 cm 的单发肝癌,我国最新多中心回顾性研究数据显示,MWA 可取得和腹腔镜肝切除术相近的 OS且更微创,而无病生存期(disease-free survival,DFS)稍逊于切除[268],尤其是对于 65 岁以上老年患者,MWA 和腹腔镜肝切除术的 DFS 无显著差异,但 OS 更高。对于 2~3 个癌灶位于不同区域,或者位居肝脏深部或中央型的肝癌,可以选择消融治疗或者手术切除联合消融治疗。
- 肝癌消融治疗后的评估和随访
局部疗效评估通常建议在消融后约 1 个月进行,通过复查动态增强 MRI/CT 扫描或超声造影评价消融效果,同时结合血清学肿瘤标志物的动态变化进行综合判断[290]。影像学评估中,若消融病灶在动脉期未见强化且未增强范围大于原病灶,提示肿瘤可能已完全坏死,可判定为完全消融;若消融病灶内或边缘在动脉期出现局部结节样强化,则提示存在肿瘤残留,属于不完全消融。对于治疗后存在肿瘤残留的患者,可考虑再次行消融治疗;若经 2 次消融后仍有肿瘤残留,则建议联合其他治疗方式。达到完全消融后,应进行规律随访,通常每 3 个月复查血清学肿瘤标志物、超声检查及动态增强MRI/CT 扫描,以便及时发现局部进展病灶或肝内新发病灶,充分发挥消融治疗微创、安全、可重复施行的优势,从而有效控制肿瘤进展。
- 人工智能在消融中的应用
人工智能及虚拟导航技术在超声引导下危险部位肝癌消融中可有助于优化消融过程及疗效,提高一次消融完全率,减少严重并发症的发生,具有较高临床应用价值。基于人工智能的个性化治疗方案将有助于选择最佳的消融治疗策略,同时降低复发率。利用深度学习和图像识别技术,可进一步提高术前影像学检查的诊断精确性,帮助医师更精准地评估肿瘤位置、大小及边界[49,51,291-296]。
要点论述:
(1)消融治疗适用于 CNLC Ⅰa 期及部分Ⅰb 期肝癌(即单个肿瘤、直径≤5 cm;或 2~3 个肿瘤、最大直径≤3 cm),可以获得根治性的治疗效果。对于不适合单纯手术切除的直径 3~7 cm 的单发肿瘤或多发肿瘤,可以消融治疗联合 TACE或手术切除。
(2)对于直径≤3 cm 的肝癌,消融治疗的 OS 类似或稍低于手术切除,但并发症发生率、住院时间低于手术切除。对于单个直径≤2 cm 肝癌,消融治疗的疗效类似于手术切除,特别是中央型肝癌。
(3)RFA 与 MWA 在早期肝癌并发症发生率以及远期生存方面,两者无显著差异,但较大肿瘤和富血供肿瘤,MWA局部完全消融疗效更佳,可以根据肿瘤的大小、位置来选择。
(4)CRA 治疗可借助超声、CT 等引导,对于≤2 cm 肝癌消融效果与微波、射频相似。
(5)PEI 对直径≤2 cm 的肝癌远期疗效与 RFA 类似。PEI的优点是安全,特别适用于癌灶贴近肝门、胆囊及胃肠道组织等高危部位,但需要多次、多点穿刺以实现药物在瘤内弥散作用。
(6)消融治疗后定期复查动态增强 MRI/CT 扫描、超声造影和血清学肿瘤标志物,以评价消融效果。
(三)经动脉介入治疗
经动脉介入治疗可根据动脉插管化疗及栓塞方式的不同进行分类,主要包括 TACE、动脉灌注化疗、SIRT 以及 TAE等治疗形式。TACE 是指将含化疗药物的碘化油乳剂或载药微球注入肿瘤供血动脉,并辅以颗粒型栓塞剂(如明胶海绵颗粒、空白微球或聚乙烯醇颗粒等)对肿瘤供血动脉分支进行栓塞,从而达到局部抗肿瘤作用。动脉灌注化疗是指经肿瘤供血动脉持续或间断灌注化疗药物的治疗方式,其中包括HAIC。常用化疗药物为蒽环类、铂类及 5-FU 类等,具体药物组合与剂量需根据患者肿瘤负荷、体表面积、肝肾功能状态、血细胞水平、体能状态、既往用药史及合并疾病等因素综合评估,并结合化疗药物的药代动力学特征合理设计灌注药物的浓度与时间[297]。SIRT 亦称经动脉放射性栓塞(transarterial radioembolization,TARE),是指经肿瘤供血动脉注射携带放射性核素的微球或其他放射性物质,以实现局部放射治疗的方式。TAE 则是单纯采用颗粒型栓塞剂对肿瘤供血动脉分支进行栓塞而不联合化疗药物。在上述多种经动脉介入治疗方式中,TACE 是目前肝癌临床应用最为广泛的方法[298-303]。
- TACE
(1)TACE 的基本原则
①要求在 DSA 机下进行;②必须严格掌握适应证和禁忌证;③必须强调超选择插管至肿瘤的供血动脉分支再进行治疗;④必须强调保护患者的肝功能;⑤必须强调治疗的规范化和个体化;⑥经过 3~4 次 TACE 治疗后,治疗的靶病灶仍处于疾病进展,应考虑更换 TACE 方案或联合其他治疗方法,如消融治疗、系统抗肿瘤治疗、放射治疗或外科手术等。
(2)TACE 的适应证
①CNLC Ⅱb、Ⅲa 期肝癌为首选治疗推荐;②预计通过TACE 治疗能控制肝内肿瘤生长而获益的 CNLC Ⅲb 期肝癌;③可手术或消融治疗,但由于其他原因(如高龄、严重肝硬化等)不能或不愿接受手术、消融或肝移植治疗的 CNLCⅠa~Ⅱa 期肝癌的替代治疗;④巨块型肝癌不能手术切除,肿瘤占全肝脏体积的比例<70%;⑤门静脉主干未完全阻塞或虽完全阻塞但存在丰富代偿性侧支血管或通过放置门静脉支架后复通门静脉血流的肝癌;⑥肿瘤破裂出血或肝动脉-门静脉分流造成门静脉高压症的肝癌;⑦存在外科术后复发的中、高危因素[肿瘤直径>5 cm、多发、合并血管或胆管癌栓、姑息性手术、术后 AFP 和(或)PIVKA‑Ⅱ等肿瘤标志物未降至正常范围等]的肝癌术后辅助治疗;⑧初始不可切除,但计划经转化或降期后为手术切除、肝移植、消融创造机会的肝癌;⑨预计肝移植等待期超过 6 个月,可采用 TACE桥接治疗的肝癌。
(3)TACE 的禁忌证
①肝功能严重障碍(Child-Pugh C 级),包括严重黄疸、肝性脑病、难治性腹水或肝肾综合征等;②无法纠正的凝血功能障碍;③门静脉主干完全闭塞,门静脉侧支代偿不足且不能通过门静脉成形术有效复通门静脉向肝血流;④肿瘤弥漫或远处广泛转移,估计生存期<3 个月;⑤ECOG PS 评分>2分、恶液质或多器官功能衰竭;⑥肾功能障碍:血肌酐>176.8μmol/L 或者血肌酐清除率<30 mL/min,且不可纠正;⑦严重碘对比剂过敏。
(4)TACE 操作程序要点和分类[304-305]
①动脉造影:全面、规范的动脉造影是 TACE 成功的基础。通常采用 Seldinger 方法,经皮穿刺股动脉(或桡动脉)等途径插管,将导管置于腹腔动脉或肝总动脉行 DSA 检查。造影图像采集应包括动脉期、实质期及静脉期,明确肿瘤部位、大小、数目及供血动脉情况。若发现肝脏区域血管稀少/缺乏或肿瘤染色不完全,应做肠系膜上动脉、胃左动脉、膈下动脉、肾动脉、胸廓内动脉、肋间动脉、腰动脉等动脉造影,以发现异位起源的肝动脉及肝外动脉侧支血管[76]。推荐使用 DSA 联合 CBCT/Angio-CT 等功能以提高肿瘤病灶显示率和供血动脉分支判断的准确性[77](证据等级 2,推荐 A)。对于严重肝硬化、门静脉主干及一级分支癌栓者,推荐经肠系膜上动脉或脾动脉行间接门静脉造影,了解门静脉血流情况 。 ② 根 据 栓 塞 剂 的 不 同 , TACE 分 为 常 规 TACE( conventional-TACE , cTACE ) 和 药 物 洗 脱 微 球 TACE(drug-eluting beads-TACE,DEB-TACE)。cTACE 是指采用以碘化油化疗药物乳剂为主,辅以明胶海绵颗粒、空白微球或聚乙烯醇颗粒等的栓塞治疗。碘化油与化疗药物需充分混合成乳剂,推荐单次用量一般不超过 20 mL。在碘化油化疗药物乳剂栓塞的基础上追加使用颗粒型栓塞剂,提高肿瘤坏死率和栓塞疗效。对局限于肝段/亚段的病灶超选择性栓塞时,以肿瘤区碘化油沉积浓密、瘤周出现门静脉小分支显影为栓塞终点;在进行肝叶水平栓塞时,在栓塞肿瘤细小供血动脉的同时保留肝段/叶动脉通畅。DEB-TACE 是指采用加载化疗药物的药物洗脱微球为主的栓塞治疗,又称载药微球TACE。载药微球通常加载蒽环类化疗药物,在栓塞肝癌供血动脉使肿瘤缺血坏死的同时作为化疗药物的载体,使化疗药物持续稳定释放,达到肿瘤局部较高血药浓度。根据肿瘤大小、血供情况和治疗目的选择不同粒径的微球,一般推荐使用小粒径微球(<100 μm、100~300 μm),血供特别丰富者可追加 300~500 μm 粒径微球。载药微球推注速度推荐 1.0mL/min,需注意微球栓塞后再分布,尽可能充分栓塞远端肿瘤滋养动脉,同时注意保留肿瘤近端供血分支,减少微球反流对正常肝组织损害[306-308]。③精细 TACE 治疗:为减少肿瘤的异质性导致 TACE 疗效的差异,提倡精细 TACE 治疗。精细 TACE 包括的关键步骤:标准化血管造影;超选择性插管至肿瘤供血动脉分支;选择合适栓塞剂;合理确定栓塞终点;TACE 后即刻评估疗效;规范的动脉造影;微导管超选择插管至肿瘤的供血动脉分支进行栓塞[309];术中采用 CBCT技术为辅助的靶血管精确插管及监测栓塞后疗效[310];栓塞材料的合理联合应用,包括碘化油、明胶海绵颗粒、空白微球、药物洗脱微球等[311];根据患者肿瘤状况、体能状态、肝功能状态和治疗目的采用不同的栓塞终点。治疗前确定个体化的TACE 治疗目标至关重要。对于局限于肝段或直径<5 cm 的肝癌,应使肿瘤完全去血管化和(或)周边门静脉小分支显影,达到肝动脉和门静脉双重栓塞效果[312-313];对于巨块型肝癌需结合患者的肝功能、体能状态、门静脉通畅等情况,尽量使肿瘤去血管化;对于肿瘤累及全肝且肿瘤负荷较高的患者,可采用分次 TACE 治疗,先处理负荷较高肝叶的肿瘤,待 2~4 周患者肝功能恢复后再处理剩余肿瘤,以减少患者肝功能损伤,提高 TACE 治疗的安全性。
精细 TACE 分为优质精细 TACE 和常规精细 TACE 两类[31469]。优质精细 TACE 的治疗目标:期望一次治疗肝内所有病灶,达到影像学完全缓解(complete response,CR)或接近CR,同时尽量减少对正常肝组织的损害。关键步骤:①适用于肝内肿瘤负荷中等的肝癌(CNLC Ⅰb、Ⅱb 期)以及无法或不愿接受根治性治疗的早期肝癌(CNLC Ⅰa 期)。②根据术前影像学检查进行标准化血管造影,评估肝癌的肝内和肝外侧支供血动脉。建议使用 CBCT/Angio-CT 等辅助术中肿瘤诊断定位及其供血动脉的确认和导航,并辅助判断栓塞终点和肿瘤活性。③使用微导管进行超选择性插管所有肿瘤供血动脉的化疗栓塞操作。④术后即刻评估效果,实现所有病灶去活性。
常规精细 TACE 的治疗目标:通过 1 次或多次 TACE 治疗使肝内经治病灶达到部分缓解(partial response,PR)或疾病稳定(stable disease,SD)。根据患者肝功能、机体状态和门静脉通畅情况,决定是否达到肿瘤完全去血管化。对于广泛肝内病灶,进行分次 TACE,随访过程中发现残余活性病灶时可进行重复 TACE。关键步骤:①适用于肝内肿瘤负荷较高的中期肝癌(CNLC Ⅱb 期)或伴血管侵犯的晚期肝癌(CNLC Ⅲ期)。②使用微导管进行超选择性插管和栓塞。③术后即刻评估效果,尽量实现大部分病灶去活性,推荐使用 CBCT/Angio-CT 等辅助血管路径导航、栓塞终点判断和肿瘤活性诊断。
(5)TACE 术后常见不良反应和并发症
TACE 治疗的最常见不良反应是栓塞后综合征,主要表现为发热、疼痛、恶心和呕吐等。发热、疼痛的发生原因是肝动脉被栓塞后引起局部组织缺血、坏死,而恶心、呕吐主要与化疗药物有关。此外,还有一过性肝功能异常、肾功能损害以及骨髓抑制等其他不良反应。一般可持续 5~7 d,经对症治疗后大多数患者能完全恢复。
并发症:急性肝、肾功能损害;消化道出血;胆囊炎和胆囊穿孔;肝脓肿和胆汁瘤形成;栓塞剂异位栓塞(包括肺和脑栓塞、消化道穿孔、脊髓损伤、膈肌损伤等)。
(6)TACE 的疗效评价
最常采用 mRECIST 单独或联合 RECIST 1.1 标准评价TACE 疗效[102,315],分为短期疗效评价和长期疗效评价。短期疗效评价指标为 ORR、PFS 等,长期疗效评价指标为 OS。基于 mRECIST 标准评估的 ORR 与 OS 有一定相关性,早期获得肿瘤客观缓解,特别是 CR 患者,预后较好[316-318](证据等级 2,推荐 B)。
(7)影响 TACE 疗效的主要因素
肿瘤分期、肿瘤负荷、肿瘤包膜完整性、肿瘤血供情况、肿瘤的病理分型、血清 AFP 水平、肝硬化程度、肝功能状态、伴慢性 HBV 感染者的血清 HBeAg 状态及 HBV DNA 水平、ECOG PS 评分以及是否联合其他治疗。
(8)随访及 TACE 间隔期间治疗
一般建议第 1 次 TACE 治疗后 4~6 周时复查动态增强CT 和(或)动态增强 MRI 扫描、肿瘤相关标志物、肝肾功能和血常规检查等;再次 TACE 治疗及后续是否需要 TACE治疗及频次应结合随访结果并遵循按需原则[319-320],主要包括患者治疗反应、肝功能和体能状况变化、影像学疗效评估及肿瘤标志物变化等,以决定是否需要再次 TACE 治疗。随访间隔 1~3 个月或更长时间,依据动态增强 CT 和(或)动态增强 MRI 扫描评价肝脏肿瘤的存活情况,以决定是否需要再次 TACE 治疗。对于大肝癌/巨块型肝癌常要 3~4 次或以上的 TACE 治疗,目前主张 TACE 联合其他治疗方法,目的是控制肿瘤、提高患者生活质量和延长生存。
(9)TACE 联合其他治疗
需重视 TACE 联合其他局部治疗和(或)系统抗肿瘤治疗,以进一步提高 TACE 疗效[298]。①在 TACE 基础上采用门静脉内支架置入术联合碘-125粒子条或碘-125粒子门静脉支架置入术,有助于恢复门静脉向肝血流、降低门静脉压力、处理门静脉主干癌栓[321-323](证据等级 2,推荐 B)。直接穿刺植入碘-125 粒子(或粒子条)可治疗门静脉一级分支癌栓[324-326](证据等级 2,推荐 B)。②TACE 联合消融治疗:为了提高 TACE 疗效,主张在 TACE 治疗基础上酌情联合消融治疗[327-328]。对不能手术切除的 CNLC Ⅰb、Ⅱa 期直径 3~7 cm的单发或多发肿瘤,效果优于单纯消融治疗[273-274,329](证据等级 2,推荐 B)。目前临床有两种 TACE 联合热消融治疗方式:序贯治疗,TACE 治疗后 1~4 周内加用消融治疗;同步治疗,TACE 治疗同时行消融治疗[327,330]。③TACE 联合外放射治疗:TACE 联合外放射治疗可提高肿瘤局部缓解率。推荐用于局限性大肝癌、伴有门静脉或下腔静脉癌栓或肝外转移的 CNLC Ⅲ期肝癌[331-332](证据等级 2,推荐 B)。④TACE联合外科治疗:TACE 可在外科治疗前作为桥接、降期或转化治疗手段,通过降低肿瘤负荷,将部分超出肝移植标准的患者转化至符合肝移植条件,从而提高肝移植率并降低术后复发和转移风险。转化成功后的肝移植患者,其总体生存与标准内患者相近[248,251,333-334](证据等级 2,推荐 B)。此外,TACE 亦可为初始不可切除肝癌创造潜在的手术切除机会,并带来长期生存获益[206]。TACE 联合 HAIC、放疗等局部治疗手段,以及靶向治疗或免疫治疗,可进一步提高转化成功率[212, 335-336](证据等级 3,推荐 B)。对于存在术后复发中、高危因素的患者,如术前肿瘤破裂、肿瘤直径>5.0 cm、多病灶、MVI 或脉管瘤栓、切缘阳性、组织分化差,或术后肿瘤标志物未降至正常水平者,推荐实施术后辅助性 TACE 治疗,以便及时发现并处理残留或复发病灶[225-227, 337-338](证据等级1,推荐 A)。SOURCE 研究证实术后 TACE 联合索拉非尼较单纯索拉非尼可显著降低合并门脉癌栓的肝癌切除患者的复发风险 43%,降低死亡风险 43%[227]。⑤TACE 联合 HAIC治疗:对于伴有门静脉主干癌栓的大肝癌(肿瘤直径≥7.0cm)、存在明显或广泛动-静脉瘘且不能良好栓塞、巨大肿瘤以及多次 TACE 治疗产生抵抗的肝癌,采用 TACE 联合 HAIC治疗能进一步提高疗效[339](证据等级 3,推荐 B)。⑥TACE联合系统抗肿瘤治疗:对于中或高肿瘤负荷、TACE 治疗后肿瘤继续进展的肝癌,应尽早联合分子靶向药物治疗[340-341]。对于晚期肝癌,TACE 联合分子靶向药物疗效优于单一分子靶向药物[209,342](证据等级 2,推荐 B)。采用 TACE 联合靶向和免疫治疗能延长中晚期肝癌患者生存期,疗效优于单一TACE 或靶向+免疫治疗[343-345]。TALENTACE 研究结果显示,对于不可切除肝癌,TACE 联合阿替利珠单抗+贝伐珠单抗患者的中位 TACE-PFS 和根据 RECIST 1.1 标准评估的中位 PFS均显著优于单独 TACE 治疗的患者(分别降低疾病进展风险29%和 36%)[346](证据等级 1,推荐 A)。LEAP-012 研究结果显示,对于不可切除的非转移性肝癌,TACE 联合仑伐替尼和帕博利珠单抗治疗患者的 PFS 显著优于接受 TACE 加安慰剂治疗的患者(降低疾病进展风险 34%)[347(] 证据等级 1,推荐 A)。对于中国人群,联合治疗组患者也有明显的临床获益,与 TACE 加安慰剂治疗相比疾病进展风险降低 47%,死亡风险降低 42%。该联合治疗方案在我国已被批准用于不可切除的非转移性肝癌的一线治疗。但最新的随访数据表明,联合治疗方案与单独使用 TACE 相比,OS 未达到统计学差异。EMERALD-1 研究结果显示,TACE 联合度伐利尤单抗和贝伐珠单抗治疗患者的中位 PFS 显著优于接受 TACE 加安慰剂治疗的患者(降低疾病进展风险 23%)[348(] 证据等级 1,推荐 A)。CARES-005(CHANCE005)Ⅱ期研究结果显示,TACE 联合卡瑞利珠单抗和阿帕替尼治疗患者的中位 PFS 和ORR 均显著优于单纯 TACE 治疗的患者(证据等级 3,推荐B)。⑦TACE 联合抗病毒治疗:对有 HBV、HCV 背景肝癌患者进行 TACE 治疗同时应积极抗病毒治疗[349-350](证据等级 1,推荐 A)。
要点论述:
(1)TACE 是肝癌最常用的经血管内介入治疗方法,主要适用于 CNLC Ⅱb~Ⅲa 期和部分 CNLC Ⅲb 期肝癌。
(2)TACE 必须遵循规范化和个体化的方案,提倡精细TACE 治疗,以减少肿瘤异质性导致的 TACE 疗效差异。
(3)对肝癌伴门静脉主干或一级分支癌栓可以在 TACE基础上联合使用门静脉内支架联合碘-125粒子条或碘-125粒子门静脉支架治疗或直接穿刺植入碘-125 粒子治疗。
(4)提倡 TACE 联合消融治疗、放射治疗、外科手术、HAIC、分子靶向药物、免疫治疗和抗病毒治疗等综合治疗,以进一步提高 TACE 疗效。
- HAIC
HAIC 主要通过肿瘤供血动脉持续灌注化疗药物来治疗肝癌,其原理是通过肝脏首过效应显著提高肿瘤局部药物浓度,同时降低全身副作用,是经动脉介入治疗肝癌的常用方法之一。传统的 HAIC 治疗多用于日本韩国等地区,采取的是低剂量顺铂为基础的方案[351]。近年来,我国学者采用以奥沙利铂、5-FU 和亚叶酸钙组成中国特色 FOLFOX-HAIC 方案显著提高了高肿瘤负荷肝癌的临床疗效[352],尤其通过提升ORR、诱导深度肿瘤退缩及促进癌栓消退,为转化性手术或消融治疗创造机会[208,353-354]。HAIC 的基本原则与 TACE 的基本原则一致(参见“TACE 的基本原则”)。由于 5-FU 的时间依赖性特征,FOLFOX-HAIC 通常需要持续灌注 23~46 h [352]。
(1)FOLFOX-HAIC 的适应证
FOLFOX-HAIC 适合于不能手术切除的大肝癌,符合下述所有条件者,考虑为 HAIC 的适应证:①肝内高肿瘤负荷,如肿瘤直径>7 cm,或影像学提示主要脉管侵犯或癌栓形成(包括部分门静脉主干完全阻塞,以及伴肝动脉-肝静脉瘘或门静脉高压的肝癌患者,仍可能从 HAIC 中获益)。②肝功能处于代偿期,肝功能 Child-Pugh 评分≤8 分。③前期未使用过含奥沙利铂的系统性治疗方案。
(2)FOLFOX-HAIC 的禁忌证
①肝内肿瘤血供贫乏,或因血管变异、闭塞等原因导致微导管无法进入;②肝功能明显异常[丙氨酸氨基转移酶(alanine aminotransferase,ALT)或天门冬氨酸氨基转移酶(aspartate aminotransferase,AST)>300 U/L,总胆红素>50μmol/L,白蛋白<28 g/L,中-大量腹水(非绝对禁忌,可经药物处理好转后进行)];③外周血白细胞和血小板显著减少,中性粒细胞<1.5×109/L,血小板<50×109/L(非绝对禁忌,如脾功能亢进者,排除化疗性骨髓抑制,可用药物处理或脾栓塞改善后进行);④无法纠正的凝血功能障碍、严重感染或合并活动性肝炎且不能有效控制者;⑤ECOG PS 评分>2 分、恶液质或多器官功能衰竭者;⑥严重碘对比剂过敏者。
(3)HAIC 操作要点
与 TACE 类似,HAIC 同样强调靶向肿瘤、保护正常组织,同样要求精细操作及超选择插管,具体如下:①规范动脉造影,全面评价肝癌血供情况:操作与 TACE 一致(参见“TACE 操作程序要点和分类”),明确肿瘤血供最丰富的供血动脉及其余分支动脉;②非靶区动脉的处理:必要时需弹簧圈栓塞胃十二指肠动脉、胃右动脉,肝左-胃交通支等非靶区血管等,避免化疗药灌注到正常组织;③肿瘤有多供血来源的处理:必要时可栓塞较小的肿瘤供血动脉,微导管超选择插管至肿瘤的血供最丰富的动脉置管进行药物灌注。
(4)FOLFOX-HAIC 术后特异性不良反应
HAIC 治疗常见的不良反应包括胃肠道反应、肝功能异常、骨髓抑制等,与 TACE 术后类似。此外 HAIC 治疗后可能出现化疗药物刺激血管引起的腹痛、一过性白蛋白下降等较为特异性的不良反应,经积极对症治疗后大多数患者能完全恢复。①奥沙利铂相关腹痛:约 30%~40%患者在奥沙利铂灌注期间出现急性上腹部疼痛,多见于肿瘤血供不丰富或血管细小,奥沙利铂刺激血管导致的痉挛性疼痛。疼痛特点为突发性、绞痛性质,多始于奥沙利铂灌注期间,通常可随停止输注奥沙利铂而缓解,约 10%~15%患者疼痛剧烈需药物干预。可予山莨菪碱、曲马多等止痛药物,疼痛剧烈者可采取肝动脉注入利多卡因溶液,腹痛能迅速得到缓解。②低白蛋白血症:接受 FOLFOX-HAIC 治疗的患者术后通常会出现较TACE 术后更为明显的低白蛋白血症,治疗期间应注意提醒患者加强营养,一般情况下 5~7 d 后可自行恢复,部分患者血清白蛋白下降明显(<30 g/L)或白蛋白轻度下降(30~35g/L)伴有腹胀水肿者可积极补充人血白蛋白。③5-FU 相关脑病:多表现为治疗后嗜睡,其机制为 5-FU 代谢产物氟柠檬酸穿透血脑屏障,抑制三羧酸循环,多见于二氢嘧啶脱氢酶(dihydropyrimidine dehydrogenase,DPD)缺乏的患者。其处理重在早期识别,FOLFOX-HAIC 治疗期间应注意观察患者情绪及神志变化,必要时急查血氨、电解质和 DPD 等,一旦发现血氨升高立即停止 5-FU 灌注;静脉注射门冬氨酸鸟氨酸、支链氨基酸、通便、乳果糖或白醋溶液灌肠等抗肝性脑病治疗;同时增加静脉补液(2 000~3 000 mL),加速 5-FU代谢。一旦确定患者为 DPD 缺乏,则需减少后续疗程 5-FU用量。④长期卧床导致的血栓/栓塞事件:关注血栓风险因素评估,对于存在中高血栓风险的患者应给予预防性抗凝治疗。
(5)治疗间隔与随访要求
FOLFOX-HAIC 一般建议间隔 3~4 周进行,每次治疗前及治疗后 1 周左右复查血常规、肝肾功能及电解质等评价安全性,每 2 次 HAIC 后复查动态增强 CT 和(或)动态增强MRI 扫描评价肿瘤疗效。根据肿瘤疗效,患者对上一次治疗的反应、肝功能和体能状况的变化等综合判断是否继续,一般连续 FOLFOX-HAIC 不超过 6 次。若肿瘤活性范围已明显减少,仅残留少许血供时应及时减少化疗药物剂量,或更换为精准 TACE 治疗,以减少化疗药物长时间灌注对大范围正常肝组织的损伤。停止 HAIC 后的随访间隔为 2~3 个月,依据动态增强 CT 和(或)动态增强 MRI 扫描评价肝脏肿瘤的存活情况,必要时补充其他方式的治疗或重启 HAIC 治疗。
(6)FOLFOX-HAIC 剂量调整
根据肿瘤大小和血供情况个体化剂量调整是减少和避免 FOLFOX-HAIC 相关不良反应的关键。肿瘤明显缩小或血供明显减少,或上 1 个疗程治疗出现 3 级以上不良事件的患者建议酌情减少化疗药物剂量。一般而言以初始剂量的 2/3为下调 1 个剂量级,最多下调 2 个剂量级,如果仍无法耐受或再次出现明显不良反应,则不再继续。①低剂量:适用于肿瘤直径<7 cm 或血供不丰富的患者,奥沙利铂 65 mg/m2、5-FU 维持 1200 mg/m2;②高剂量:适用于肿瘤直径≥7 cm 且血供丰富的患者,奥沙利铂 85 mg/m2、5-FU 首剂 400 mg/m2维持 2400 mg/m2[对于肿瘤特别巨大或血供极其丰富的肿瘤,首 次 可 采 取 奥 沙 利 铂 130 mg/m2 。 灌 注 时 间 : 最 初 的FOLFOX-HAIC 采用 46 h 5-FU 持续动脉输注方案。近年来基于改善耐受性的考虑,多个中心开始采用 23 h 5-FU 动脉输注方案(总剂量不变)。有研究指出与标准 46 h 方案相比,23 h 方案的有效性和安全性无显著差异[355]]。
(7)FOLFOX-HAIC 治疗暂停/终止标准
①3 级不良事件:暂停灌注,积极对症处理,下个周期调整剂量;②除可逆性骨髓抑制及肝功能异常以外的 4 级不良事件,终止 HAIC 治疗;③肝内病灶进展:停止 HAIC,或联合其他治疗,如 TACE 及系统性药物治疗。
(8)FOLFOX-HAIC 与其他治疗联合
①转化治疗:对于 CNLC Ⅱb、Ⅲa 期的局部晚期肝癌,特别是巨块型肝癌或合并门静脉癌栓者,FOLFOX-HAIC 单用或联合靶向/免疫治疗可提高生存率和转化切除率[356-358](证据等级 3,推荐 B)。采用 HAIC 转化治疗的优选标准为:单发肿瘤,或多发肿瘤位于肝脏一侧;无门静脉主干或下腔静脉癌栓,无肝外转移;ECOG PS 评分 0~1 分,肝功能Child-Pugh A 级[359-360]。末次 HAIC 后 3~4 周是理想的手术窗口期,若联合抗血管生成药物(如贝伐珠单抗),则需延长至至少 6 周后。②联合靶向及免疫治疗:FOLFOX-HAIC 联合索拉非尼较单用索拉非尼显著提高生存率(尤其门静脉癌栓患者)[208](证据等级 2,推荐 B)。采用 HAIC+靶向+程序性死亡受体 1(programmed death-1,PD-1)抑制剂的三联方案在晚期肝癌中显示出更优疗效,ORR 可达 64%~77%[357-358](证据等级 2,推荐 B)。③FOLFOX-HAIC 与 TACE 联合:适用于多发性肝癌,尤其当病灶存在多支血供或异常丰富血供,或病灶分散于左、右肝时,可采用 TACE 栓塞其中部分供血动脉,而 HAIC 则灌注主要供血动脉[212, 361(] 证据等级 3,推 荐 B )。 ④ 肝 内 病 灶 为 主 伴 肝 外 寡 转 移 : 单 一FOLFOX-HAIC 可作为一线选择,有效控制肝内病灶的同时对转移灶也有一定抑制作用,有研究表明对于晚期肝癌,FOLFOX-HAIC 疗效显著优于索拉非尼[207,354](证据等级 2,推荐 B)。⑤新辅助治疗:对于具有高复发风险特征的可切除肝癌,术前新辅助 HAIC 治疗可降低术后复发和死亡风险,为患者争取更长的无瘤生存期[362](证据等级 2,推荐 B)。⑥术后高风险复发患者:对于肝切除术后存在 MVI 的患者,HAIC 辅助治疗可显著降低术后复发风险[229](证据等级 2,推荐 B)。
要点论述:
(1)采用以奥沙利铂、5-FU 和亚叶酸钙组成中国特色FOLFOX-HAIC 方案显著提高了高肿瘤负荷肝癌的临床疗效。
(2)FOLFOX-HAIC 适合于多次 TACE 治疗产生抵抗、肝内高肿瘤负荷、肝癌合并主要脉管侵犯或癌栓形成的患者。
- SIRT
SIRT 是指采用经皮穿刺将导管插管至肿瘤供血动脉内,注射带有放射性核素的物质,通过放射性核素释放高能量射线(β射线)在肿瘤局部聚集,持续近距离照射毁损并杀灭肿瘤,从而达到控制肿瘤生长的治疗方法,属内放射范畴。最常用的放射性微球为钇-90(90Y)微球。根据载体不同,90Y 微球主要分为玻璃微球(TheraSphere)、树脂微球(SIR-Sphere)、可视化玻璃微球(Eye90 microspheres)和炭微球(TareSphere)。其中,TheraSphere 于 1999 年获美国食品药品管理局(FDA)批准用于不可手术切除肝癌的治疗,SIR-Sphere 分别于 2002 年和 2025 年获得 FDA 批准用于“联合氟脲苷动脉化疗治疗不可手术切除的结直肠癌肝转移”和“不可手术切除肝癌”的治疗。Eye90 microspheres 于 2022 年获 FDA 批准用于动静脉畸形和高血管肿瘤的治疗。在欧洲、亚洲部分国家和地区 SIRT 还被批准用于治疗其他不适合手术切除的肝脏恶性肿瘤的治疗。SIRT 一般需要由介入放射科、肝脏外科、核医学科、放射肿瘤科、肿瘤内科、影像科等组成的 MDT 共同完成。
(1)SIRT 的临床应用范围
肝 癌 患 者 SIRT 的 临 床 适 用 人 群 应 满 足 : 肝 功 能Child‑Pugh A 或 B 级、ECOG PS 评分 0~2 分。具体应用范围包括:①因合并症不能或不愿接受根治性治疗的 CNLCⅠa~Ⅱa 期肝癌;②因 FLR 不足,无法行手术切除的 CNLCⅠb、Ⅱa 期肝癌;③肝癌肝移植前桥接治疗;④初治或其他治疗后复发及进展的多发性病灶、肿瘤负荷高、伴有门静脉癌栓的 CNLC Ⅱb、Ⅲa 期肝癌;⑤伴有肝外转移的肝癌,可联合系统治疗进行姑息性治疗。
(2)SIRT 禁忌证
①肝功能严重障碍(Child‑Pugh C 级);②严重凝血功能障碍;③合并严重感染且不能有效控制;④肿瘤弥漫或远处广泛转移,预期生存期<3 个月;⑤ECOG PS 评分>2 分、恶液质或多器官功能衰竭;⑥肾功能障碍:血肌酐>176.8μmol/L 或肌酐清除率<30 mL/min,且不可纠正;⑦肺部单次吸收剂量>30 Gy(合并肺基础疾病时>20 Gy),或累积吸收剂量>50 Gy;⑧存在不能预处理的危险动脉或分流而导致90Y 微球肝外异位分布风险;⑨治疗区域的正常肝实质所受辐射剂量过大(肝脏正常时超过 70 Gy,肝硬化时超过 50Gy)
(3)SIRT 操作程序及要点
SIRT 操作具体按照精细 TACE 原则要求进行,并需包括以下流程:①血管造影:一般在 SIRT 前的 2 周内完成,推荐在 CBCT 辅助引导下进行,明确肿瘤治疗区域的动脉供血情况,寻找和识别造成非靶器官放射性损伤的高风险动脉分支[363]。对于存在可能导致 90Y 异位分布的动脉,可采用预防性栓塞或通过超选择血管插管以避开上述风险血管,或采用球囊微导管避免反流。对于肿瘤治疗靶区存在的肝动脉-肝静脉瘘,若能明确瘘口所在动脉且不影响较大治疗区域的情况下,可考虑先对瘘口进行封堵。最后精准确定导管头端位置及形态,有效判断覆盖区域肿瘤病灶特征,及 90Y 可能影响的正常肝组织。②99mTc 聚合白蛋白(99mTc labledmacroaggregated albumin,99mTc-MAA)模拟:是 SIRT 的关键步骤,用于评估 90Y 微球的分布和安全性。在明确肿瘤供血动脉并将微导管头端置于拟行 SIRT 的位置后,将 2~5 mCi(5~10 mL)的 99mTc-MAA 注射至肿瘤治疗区域。推荐在99mTc-MAA 标记后2 h 内注射,注射后2 h 内进行SPECT/CT显像,以降低 99mTc-MAA 脱标和清除造成的影响,并分析肝、肺及胃肠区域放射性分布[364]。③90Y 处方剂量计算:根据治疗目的(根治性、桥接、降期/转化或姑息性治疗)、肿瘤特征、非靶器官(肺、正常肝组织、其他可能危及的器官等)剂量限值、患者一般状况、肝功能状况、是否联合其他治疗、肝-肺分流等因素来综合计算。肿瘤接受剂量以及非瘤肝实质所受辐射剂量限定如下:对于 SIR-Sphere:正常肝脏组织≤70 Gy,伴有肝硬化时≤40~50 Gy;肺部所受辐射剂量≤30 Gy,并应尽量<20 Gy,累计吸收剂量≤50 Gy [365]。推荐在非靶区吸收剂量安全范围内尽可能提高肿瘤的处方剂量,建议最低 100~120 Gy 以上。对于 TheraSphere,推荐肿瘤吸收剂量在 205 Gy 以上[366-367]。④SIRT 实施:注射 90Y 时需保持微导管头端位置与注射 99mTc-MAA 时的位置一致。注意排出注射管路中的气泡,检查并确认注射管路的通畅性和密闭性。输注完毕,将导管、剂量瓶、输注管道和接触敷料回收至核废物专用罐。术后及时核医学检查评估靶区与危及器官剂量。
(4)SIRT 常见不良反应和并发症
SIRT 常见不良反应包括一过性疲劳、恶心、厌食、腹痛及低热,通常为自限性,支持治疗即可。严重并发症主要是90Y 微球异位分布引起的组织或器官的放射性损伤,包括:放射性上消化道损伤、放射性肝炎、放射性胆囊炎/胆管损伤、放射性肺炎、放射性皮炎等[368]。
(5)SIRT 疗效评价
SIRT 最常用的疗效评价指标是 PFS、ORR、疾病进展时间和 OS。影像评估手段推荐动态增强 CT/动态增强 MRI。SIRT 术后 12 周建议进行 PET/CT 检查。优先推荐 mRECIST标准,其次是 RECIST 1.1 标准等。由于 SIRT 治疗后引起瘤周水肿和出血等影像学改变可能被误认为浸润型肿瘤病灶,并误认为肿瘤体积增大进展,因此 mRECIST 标准能更早地准确评价 SIRT 治疗效果。
(6)SIRT 随访及治疗间隔
SIRT 术后随访应包括患者一般情况、体能状况、血常规、肝肾功能、肿瘤标志物、影像学检查、不良反应等。推荐 SIRT术后 6~12 周进行首次随访,随后每 2~3 个月复查 1 次。SIRT术后 3~6 个月可因残存活性病灶或病灶局部进展,可考虑再次行 SIRT 治疗。
(7)SIRT 联合其他治疗
SIRT 单独应用于肝癌的疗效已经得到多项临床研究的初步证实。对于孤立性,肿瘤直径≤8 cm、肝功能 Child-PughA 级、ECOG PS 评分 0~1 分的不可切除肝癌,患者 3 年 OS为 86.6%,ORR 为 88.3%,62.2%的患者 6 个月内疾病无进展[369](证据等级 3,推荐 C)。对于直径≤3.0 cm、肝功能Child-Pugh 评分≤7 分、ECOG PS 评分 0 分,无转移或大血管侵犯的孤立性肝癌进行放射性肝段切除治疗,CR 率为83%,PR 率为 17%[370](证据等级 3,推荐 C)。另有研究表明,对 TACE 治疗反应不佳者行 SIRT 治疗是安全有效的[371](证据等级 3,推荐 C)。数项单臂、Ⅱ期试验探索了 SIRT术后 3 周联合纳武利尤单抗、度伐利尤单抗和帕博利珠单抗治疗中晚期肝癌,证实了该联合治疗的安全性和有效性[371-374](证据等级 3,推荐 C)。目前,SIRT 联合系统治疗及 SIRT行降期和转化治疗的多项临床研究也在进行中。未来,SIRT治疗应侧重构建可预测 SIRT 放射敏感性和生存获益的模型,实现真正意义上的个体化施治;探索 SIRT 与系统治疗的协同机制;开发基于肿瘤异质性和个体特征的生物有效剂量模型;拓展不同临床应用场景;优化 SIRT 治疗的全程管理
要点论述:
(1)SIRT 操作具体按照精细 TACE 原则要求进行。
(2)SIRT 一般需要由介入放射科、肝脏外科、核医学科、放射肿瘤科、肿瘤内科、影像科等组成的 MDT 共同完成。
(四)放射治疗
放射治疗分为外放射治疗和内放射治疗。外放射治疗是利用放疗设备产生的射线(光子或粒子)从体外进入体内对肿瘤照射。内放射治疗是利用放射性核素,经机体管道或通过针道植入肿瘤内。肝癌对放射敏感,中等剂量的放射治疗,就可以获得较好的肿瘤反应率。
- 外放射治疗
(1)外放射治疗适应证
①CNLC Ⅰa、部分Ⅰb 期肝癌,如无手术切除或消融治疗适应证或不愿接受有创治疗,可以酌情考虑采用 SBRT 作为替代的治疗手段[375-384(] 证据等级 2,推荐 B)。②CNLC Ⅱa、Ⅱb 期肝癌,TACE 联合外放射治疗,可改善局部控制率[385]、延长生存时间,较单用 TACE、索拉非尼或 TACE 联合索拉非尼治疗的疗效好,可以适当采用[331,377,386-392](证据等级 2,推荐 B)。③CNLC Ⅲa 期肝癌,对于可切除的伴门静脉癌栓肝癌,行术前新辅助放射治疗[393]或术后辅助放射治疗,延长生存[166,394](证据等级 2,推荐 B);对于不能手术切除者,可行姑息性放射治疗,或放射治疗与 TACE 等联合治疗,尤其 TACE 前放射治疗,可显著延长患者生存[331,391-392,395-396(] 证据等级 2,推荐 B)。④CNLC Ⅲb 期肝癌,部分寡转移灶者,可行 SBRT,延长生存时间[397];淋巴结、肺、骨、脑或肾上腺等转移灶,放射治疗可以减轻转移灶相关疼痛、梗阻或出血等症状,延长生存时间[332,398-400](证据等级 3,推荐 A)。⑤放射治疗可与手术联合,能改善部分肝癌患者生存。放射治疗可用于等待肝癌肝移植术前的桥接治疗[401-402](证据等级 2,推荐 B);部分中央型肝癌可行术前新辅助放疗,其疗效较好且患者耐受性佳[403];放射治疗可联合介入或免疫药物治疗[336],使部分无法手术切除的肝癌,在肿瘤缩小或降期后转化为手术切除[332,379];肝癌术后病理示有 MVI 者、肝癌手术切缘距肿瘤≤1 cm 的窄切缘者,术后辅助放射治疗可以减少病灶局部复发或远处转移、延长患者无瘤生存期[404-407(] 证据等级 2,推荐 B)。⑥放射治疗可与分子靶向类、免疫类药物治疗联合:部分 CNLC Ⅲ期或伴 MVI 等不良预后因素的患者,放射治疗前[408]、治疗后使用索拉非尼[409]、仑伐替尼[410]等分子靶向药可能延长生存[411-413],但同步使用这类药物须谨慎[414-415];ICIs 联合 SBRT 治疗肝癌,有研究结果提示可能起到相互协同增效的作用[416-420];SBRT 可联合仑伐替尼及PD-1 抑制剂,较仅联合仑伐替尼,可改善不可切除肝癌患者的生存[421];对于合并门静脉癌栓的患者,放射治疗联合免疫及抗血管生成药物的三联疗法可延长生存[422],且未增加额外毒性(证据等级 3,推荐 C)。
(2)外放射治疗禁忌证
肝内病灶弥散分布或 CNLC Ⅳ期肝癌,不建议行外放射治疗,除外肝移植前的桥接治疗。
(3)外放射治疗实施原则与要点
肝癌外放射治疗实施原则为综合考虑肿瘤照射剂量,周围正常组织耐受剂量,以及所采用的放射治疗技术。肝癌外放射治疗实施要点为:①放射治疗计划制定时,肝内病灶在增强 CT 中定义,建议参考 MRI 影像等多种影像资料;必要时利用正常肝组织的增生能力,可在放射治疗时保留部分正常肝不受照射,以期该部分肝组织获得增生。②肝癌照射剂量,与患者生存时间及局部控制率密切相关,基本取决于周边正常组织的耐受剂量[213,423]。肝癌照射剂量:SBRT 一般推荐≥30~60 Gy/3~10 分次(Fraction,Fx)[379,423-424]、放射治疗生物等效剂量(biological effective dose,BED)≥80 Gy(α/β比值取 10 Gy),病灶可获得较好的放疗效果[376];常规分割放射治疗为 50~70 Gy;新辅助放射治疗门静脉癌栓的剂量可以为 3 Gy×6 Fx [166]。具有图像引导放射治疗(image guidedradiation therapy,IGRT)技术条件者,部分肝内病灶、癌栓或肝外淋巴结、肺、骨等转移灶可行低分割放射治疗者尽量采用低分割放疗,以提高单次剂量、缩短放射治疗时间、疗效不受影响甚至可以提高[425-427];非 SBRT 的低分割外放射治疗,可以利用模型计算 BED,有 HBV 感染患者的肝细胞α/β比值取 8 Gy,肿瘤细胞α/β比值取 10~15 Gy,作为剂量换算参考[213,332,428]。③正常组织耐受剂量需考虑:放射治疗分割方式、肝功能 Child-Pugh 分级、正常肝(肝脏-肿瘤)体积[429]、胃肠道瘀血和凝血功能状况等(附录 8)。④肝癌放射治疗技术:建议采用三维适形或调强放射治疗、IGRT或SBRT等技术。IGRT 优于非 IGRT 技术[423],螺旋断层放射治疗适合多发病灶的肝癌。呼吸运动是导致肝脏肿瘤在放射治疗过程中运动和形变的主要原因,目前可以采取多种技术以减少呼吸运动带来的影响,如门控技术、实时追踪技术、呼吸控制技术以及腹部加压结合 4D-CT 确定内靶区技术等[430]。⑤目前缺乏较高级别的临床证据以支持肝癌患者质子放射治疗的生存率优于光子放射治疗。
(4)放疗疗效评估
肝癌放疗的疗效可以参考 mRECIST 标准进行评价。CT/MR 增强扫描常用来评价肝癌放疗后疗效。放疗后早期(3周至 3 个月)肿瘤多为凝固坏死,缩小缓慢,疗效评价多为SD[431];放疗后期(约 3~6 个月后),肿瘤坏死被逐渐吸收表现为肿瘤明显缩小,平均可缩小 36%以上,肿瘤动脉期强化显著降低或不强化[432]。
(5)外放射治疗主要并发症
放射性肝病(Radiation-induced liver diseases,RILD)是肝脏外放射治疗的剂量限制性并发症,分为典型性和非典型性两种:①典型 RILD:碱性磷酸酶(AKP)升高>2 倍正常值上限、无黄疸性腹腔积液、肝肿大;②非典型 RILD:AKP>2倍正常值上限、ALT>正常值上限或治疗前水平 5 倍、肝功能Child-Pugh 评分恶化≥2 分,但是无肝肿大和腹腔积液。诊断RILD 必须排除肝肿瘤进展、病毒性或药物性所致临床症状和肝功能损害[332,429]。临床影像学所见局灶放射性肝损伤是对应于肝脏受到较高剂量照射的区域,如在此基础上出现 RILD 相关临床症状体征、实验室指标异常,并需临床干预治疗,才可诊断RILD。早期,局灶放射性肝损伤 CT 表现多为边界清楚肝内低密度区,MRI 表现为 T1WI 低信号/T2WI 高信号,TIWI增强动脉期强化下降[431]。晚期,增强 CT 或 MRI 均表现为病变区局部萎缩、动脉及延迟期呈不均质强化,该强化退出缓慢[433-435],随访时需与局部复发或进展相鉴别[332,436]。
- 质子束放射疗法与内放射治疗
质子束放射疗法(proton beam radiotherapy, PBT)凭借“布拉格峰”剂量学优势,理论上能更好地保护肿瘤照射野后方紧邻的关键组织,可应用于治疗紧邻脊髓、肝门或胃肠道等特殊位置的肝癌。PBT对于术后复发或残留肝癌病灶(肿瘤直径<3 cm,数目≤2 个)的疗效与 RFA 相似[437](证据等级 2,推荐 C)。PBT 对呼吸运动敏感;肝功能严重不全、肝内病灶数目过多或呈弥漫性,以及肝外广泛转移等情况亦是PBT 的相对禁忌证。
内 放 射 治 疗 是 局 部 治 疗 肝 癌 的 一 种 方 法 , 包 括90Y-SIRT、碘-131 单抗、放射性碘化油、碘-125 粒子植入等[399-400];由于“由内而外”的照射方式,其剂量分布遵循“距离平方反比定律”,即剂量随照射源距离迅速衰减,理论上可使肿瘤内受到致死性高剂量照射,而肿瘤边缘外剂量骤降,有效保护紧邻的重要器官。RFA 治疗肝癌后序贯使用碘[131I]美妥昔单抗治疗,可以降低 RFA 治疗后局部复发率,改善患者生存[438](证据等级 2,推荐 C)。粒子植入技术包括组织间植入、门静脉植入、下腔静脉植入和胆道内植入,分别治疗肝内病灶、门静脉癌栓、下腔静脉癌栓和胆管内癌或癌栓。氯化锶(89Sr)发射出β射线,可以用于靶向治疗肝癌骨转移病灶[439](证据等级 3,推荐 C)。肝功能严重不全、不可纠正的肝-肺分流、肝外广泛转移、乏血供肿瘤是内放射治疗的相对禁忌证。
要点论述:
(1)CNLC Ⅲa 期可切除肝癌,行术前新辅助放射治疗或术后辅助放射治疗,可以延长生存;对于不能手术切除肝癌,行姑息性放射治疗,或放射治疗与 TACE 等联合治疗,延长患者生存。
(2)CNLC Ⅲb 期肝癌,部分寡转移灶者,可行 SBRT,延长生存时间;淋巴结、肺、骨、脑或肾上腺转移可采用放射治疗减轻疼痛、梗阻或出血等症状。
(3)放射治疗与手术、分子靶向类或免疫类药物治疗联合使用。
(4)肝肿瘤照射剂量:SBRT 一般推荐剂量≥30~60Gy/3~10 Fx,常规分割放射治疗剂量一般为 50~75 Gy,照射剂量与患者生存密切相关。部分肝内病灶或肝外转移灶可行低分割放射治疗,以提高单次剂量、缩短放射治疗时间。
(5)正常组织的耐受剂量必须考虑:放射治疗分割方式、肝功能 Child-Pugh 分级、正常肝(肝脏-肿瘤)体积、胃肠道瘀血和凝血功能状况等。
(6)IGRT 优于三维适形放射治疗或调强放射治疗,SBRT 必须在 IGRT 下进行。
(7)内放射治疗是肝癌局部治疗的一种方法。
(五)系统治疗
系统治疗(或称全身性治疗)是中晚期肝癌的重要治疗手段,主要是抗肿瘤治疗,包括分子靶向药物、ICIs、系统化疗和中医中药治疗等;另外,还有针对基础肝病的系统治疗,包括抗病毒、保肝利胆、防治并发症和对症支持治疗。
由于大多数患者存在基础肝病(肝炎、肝硬变、肝功能异常以及相关并发症),肝癌起病隐匿,早期症状不典型,首次诊断时仅有 20%~30%的肝癌患者适合接受根治性治疗(手术和其他局部治疗),因此系统治疗在中晚期肝癌的治疗过程中发挥着不可或缺的作用。系统治疗的目标为控制患者的疾病进展、减轻症状、改善生活质量和延长生存时间;部分患者可以获得肿瘤 PR 或 CR[440-441](证据等级 1,推荐A)。
系统治疗用于不可手术切除的中晚期肝癌中的适应证:CNLC IIIa、IIIb 期肝癌患者;不适合手术切除或 TACE 治疗的 CNLC IIb 期肝癌患者;TACE 治疗抵抗或 TACE 治疗失败的肝癌患者;可以与经动脉介入治疗联合,治疗 CNLC 分期IIb、IIIa、IIIb 期的肝癌。
- 一线系统治疗
一线治疗推荐用于既往未接受过系统性治疗的不可切除或转移性 HCC 患者。基于多项Ⅲ期临床研究,免疫联合方案(如 ICIs 联合抗血管生成药物或双免疫联合)的疗效显著优于索拉非尼或仑伐替尼单药,已经成为优先选择。
(1)阿替利珠单抗联合贝伐珠单抗:在全球多国获批用于既往未接受过系统抗肿瘤治疗的不可切除肝癌患者(证据等级 1,推荐 A)。IMbrave150 全球多中心的Ⅲ期临床研究[440-441]结果显示,阿替利珠单抗联合贝伐珠单抗组的 mOS 和中位无进展生存时间(median progression free survival,mPFS)较索拉非尼组均有明显延长。联合方案可降低死亡风险 34%,mOS 达到 19.2 个月,优于索拉非尼组的 13.4 个月(HR=0.66,95% CI=0.52~0.85);疾病进展风险降低 35%,联合治疗组 mPFS 为 6.9 个月优于索拉非尼组 4.3 个月(HR=0.65,95% CI=0.53~0.81)。中国亚组人群 mOS 为 24.0个月,同样明显优于索拉非尼组的 11.4 个月,降低死亡风险47%(HR=0.53,95% CI=0.35~0.80)。联合治疗组的 mPFS为 5.7 个月,索拉非尼组为 3.2 个月,疾病进展风险降低 40%(HR=0.60,95% CI=0.40~0.90)。联合治疗组 ORR 达到27.3%,明显高于索拉非尼组的 11.9%。同时联合治疗延迟了患者报告的中位生命质量恶化时间。常见的不良反应有高血压、蛋白尿、肝功能异常、腹泻以及食欲下降等。注意事项:治疗前需进行胃镜检查评估静脉曲张出血风险;禁用于严重出血或重度肝功能不全(肝功能 Child-Pugh C 级)患者。
(2)纳武利尤单抗联合伊匹木单抗:已在多国获得批准一线治疗不可切除或晚期肝癌成人患者(证据等级 1,推荐 A)。CheckMate-9DW 随机对照、全球多中心的Ⅲ期研究[442]结果显示,纳武利尤单抗联合伊匹木单抗双免联合治疗组mOS 为 23.7 个月,研究者选择的仑伐替尼/索拉非尼组(85%仑伐替尼/15%索拉非尼)为 20.6 个月(HR=0.79,95%CI=0.65~0.96,P=0.0180),降低 21%的死亡风险。联合治疗组总人群 3 年 OS 率为 38%。双免联合治疗组 mPFS 为 9.1个月,仑伐替尼/索拉非尼组为 9.2 个月(HR=0.87,95%CI=0.72~1.06)疾病进展风险降低 13%。此外,纳武利尤单抗加伊匹木单抗组的 ORR 也显著高于仑伐替尼/索拉非尼组(36% vs. 13%,P<0.0001)。联合治疗组常见的不良反应为瘙痒,转氨酶升高、皮疹和腹泻。注意事项:需要监测免疫相关不良反应(immune-related adverse events,irAEs),基础肝病严重、肝功能较差者应慎用(Child-Pugh B 级中≥8 分的 3~4 级肝毒性发生率为 18.7%)。
(3)阿帕替尼联合卡瑞利珠单抗:在我国批准用于不可切除或转移性肝癌患者的一线治疗(证据等级 1,推荐 A)。CARES-310 国际多中心的Ⅲ期研究[443]结果显示,阿帕替尼联合卡瑞利珠单抗组与索拉非尼单药组相比,两组的 mOS分别为 23.8 个月与 15.2 个月(HR=0.64,95% CI=0.52~0.79,P<0.0001),即联合治疗组使得死亡风险降低 38%,2 年 OS率达到 49.0%,3 年 OS 率达到 37.7%,显著高于对照组的36.2%和 24.8%;两组的 mPFS 分别为 5.6 个月与 3.7 个月(HR=0.54,95% CI=0.44~0.67,P<0.0001),即疾病进展风险下降 48%;显示出持续的具有临床意义的生存改善;同时,客观有效率分别为 26.8% vs. 5.9%,安全性可控。联合治疗组常见的不良反应有高血压、蛋白尿、AST 及 ALT 升高等。注意事项:卡瑞利珠单抗单药使用时引起反应性皮肤毛细血管 增 生 症 ( reactive cutaneous capillary endothelialproliferation,RCCEP)的发生率较高,但是联合用药后显著下降。2025 年,该方案已经获得欧洲肿瘤内科学会(ESMO)指南和 BCLC 指南的收录和推荐
(4)信迪利单抗联合贝伐珠单抗类似物:在我国批准用于既往未接受过系统抗肿瘤治疗的不可切除或转移性肝癌的一线治疗(证据等级 1,推荐 A)。ORIENT-32 全国多中心Ⅲ期研究[444]结果显示,联合治疗组的 OS 显著优于索拉非尼组,mOS 在联合治疗组未达到,索拉非尼组为 10.4 个月(HR=0.57,95% CI=0.43~0.75,P<0.0001),死亡风险下降43%。联合治疗组的 mPFS 也显著优于索拉非尼,两组 mPFS分别为 4.5 个月和 2.8 个月(HR=0.56,95% CI=0.46~0.70,P<0.0001),联合治疗组疾病进展风险下降 44%。按照 RECIST1.1 标准评估,两组 ORR 分别为 21%和 4%。联合方案安全性较好,联合治疗组最常见的不良反应有高血压、蛋白尿、AST 及 ALT 升高等。
(5)菲诺利单抗联合贝伐珠单抗:在我国批准用于既往未接受过系统抗肿瘤治疗的不可切除或转移性肝癌患者(证据等级 1,推荐 A)。SCT-I10A-C301 全国多中心Ⅲ期研究[445]结果显示,与索拉非尼单药相比,菲诺利单抗联合贝伐珠单抗组(联合组)mOS 显著长于索拉非尼组(22.1 个月vs.14.2 个月,HR=0.60,95% CI=0.44~0.81,P=0.0008),死亡风险降低40%。联合组的mPFS也显著优于索拉非尼组(7.1个月 vs. 2.9 个月,HR=0.50,95% CI=0.38~0.65,P<0.0001),疾病进展风险降低 50%。联合组的 ORR 高于索拉非尼组(32.8% vs. 4.3%)。联合组最常见的不良反应是蛋白尿、血小板减少、AST 升高、胆红素升高等。注意事项可参考阿替利珠单抗联合贝伐珠单抗。
(6)特瑞普利单抗联合贝伐珠单抗:在我国批准用于未接受过系统抗肿瘤治疗的不可切除或转移性肝癌患者(证据等级 1,推荐 A)。HEPATORCH 全国多中心Ⅲ期研究[446]结果显示,特瑞普利单抗联合贝伐珠单抗联合治疗组能够显著提升肝癌患者生存获益。联合治疗组 mPFS 为 5.8 个月,索拉非尼组为 4.0 个月(HR=0.69,95% CI=0.53~0.91,P=0.0086),降低疾病进展风险达 31%。联合治疗组 mOS 为20.0 个 月 , 索 拉 非 尼 组 为 14.5 个 月 ( HR=0.76 , 95%CI=0.58~0.99,P=0.0394)降低死亡风险达 24%。联合治疗组最常见不良反应是蛋白尿、血小板减少、低蛋白血症和高血压等。注意事项可参考阿替利珠单抗联合贝伐珠单抗。
(7)安罗替尼联合派安普利单抗:在我国批准用于既往未接受过系统抗肿瘤治疗的不可切除或转移性肝癌的治疗(证据等级 1,推荐 A)。APOLLO 全国多中心Ⅲ期临床研究[447]的结果显示,安罗替尼联合派安普利单抗对比索拉非尼一线治疗晚期肝癌患者,联合治疗组疾病进展风险下降47%,死亡风险下降 31%。联合治疗组常见的不良反应有高血压、血小板计数降低、AST 升高、血胆红素升高等。
(8)多纳非尼:在我国批准用于既往未接受过系统性抗肿瘤治疗的不可切除肝癌患者(证据等级 1,推荐 A)。ZGDH3 全国多中心Ⅲ期研究[448]结果显示:与索拉非尼相比,多纳非尼达到了优效的结局,明显延长晚期肝癌的生存时间,两组 mOS 分别为 12.1 个月与 10.3 个月(HR=0.831,95%CI=0.699~0.988,P=0.0247),死亡风险下降 17%;18 个月OS 率分别为 35.4%与 28.1%;同时,多纳非尼在 ORR、疾病控制率(disease control rate,DCR)、中位疾病进展时间(median time to progress,mTTP)和 mPFS 方面,均较索拉非尼有明显的改善趋势。多纳非尼具有良好的安全性和耐受性。常见不良反应为手足皮肤反应、AST 升高、总胆红素升高、血小板降低和腹泻等。
(9)仑伐替尼:适用于既往未接受过系统抗肿瘤治疗的不可切除的肝癌患者(证据等级 1,推荐 A)。REFLECT国际多中心Ⅲ期临床研究[449]结果数据显示,其 mOS 非劣于索 拉 非 尼 , 研 究 达 到 非 劣 效 终 点 ( HR=0.92 , 95%CI=0.79~1.06);mPFS 显著优于索拉非尼组,疾病进展风险下降 34%,ORR 也高于索拉非尼。常见不良反应为高血压、蛋白尿、腹泻、食欲下降、疲劳、手足综合征等。
(10)替雷利珠单抗:在我国获得批准单药用于不可切除或转移性肝癌的一线患者(证据等级 1,推荐 A)。97RATIONALE-301 全球多中心Ⅲ期研究[450]结果显示,与索拉非尼相比,达到了预设的主要研究终点,mOS 为非劣效性,两组的 mOS 分别为 15.9 个月和 14.1 个月(HR=0.85,95%CI=0.71~1.02),死亡风险降低了 15%,具有生存获益的趋势。同时替雷利珠单抗组的安全性更优。常见不良反应为 AST 升高、ALT 升高和总胆红素升高。
(11)索拉非尼:索拉非尼是全球第一个获批用于肝癌系统抗肿瘤治疗的分子靶向药物。两项国际临床研究[451-452]表明,索拉非尼对于不同国家地区、不同肝病背景的晚期肝癌患者都具有一定的生存获益(证据等级 1,推荐 A)。索拉非尼可用于肝功能 Child-Pugh A/B 级的患者,但是肝功能Child-Pugh A 级的患者生存获益比较明显[453]。治疗过程中应定期评估疗效和监测毒性。常见的不良反应为腹泻、手足综合征、皮疹、高血压、食欲缺乏以及乏力等,一般发生在治疗开始后的 2~6 周内。
(12)系统化疗:奥沙利铂为主的系统化疗(FOLFOX4方案)在我国获得批准用于一线治疗不适合手术切除或局部治疗的局部晚期和转移性肝癌,EACH 国际多中心Ⅲ期研究[454-455]首次证明含奥沙利铂的系统化疗方案可以为晚期肝癌患者带来局部控制和生存获益,与对照组多柔比星相比,FOLFOX4 组 mOS 具有明显优势(6.47 个月 vs. 4.90 个月,P=0.0425),即可降低死亡风险达 21.5%(证据等级 1,推荐A)。
(13)其他一线系统抗肿瘤治疗进展:
HIMALAYA 研究是全球首个获得成功的国际多中心的Ⅲ期临床研究[456-457](证据等级 1,推荐 B),其结果显示,与索拉非尼对比,PD-L1 抑制剂度伐利尤单抗联合 CTLA-4抑制剂替西木单抗(STRIDE 方案:单次给药 300 mg 替西木单抗+度伐利尤单抗 1500 mg 每 4 周 1 次常规间隔给药)具有较好的临床疗效和可控的安全性,降低死亡风险 24%。STRIDE 方案使得亚洲(除日本以外)患者死亡风险降低了24%,其中 HBV 阳性患者的死亡风险降低了 34%。STRIDE方案已经获得美国 FDA、欧盟药品管理局和日本药品管理局批准,可用于治疗不可切除的肝癌患者,但是该方案在我国尚待国家药品监督管理局批准。另外,在 HIMALAYA 研究[456]中,度伐利尤单抗与索拉非尼相比达到了预设的非劣效终点,死亡风险降低了 14%,且安全性更好。
目前,多项 ICIs 单药/双免疫联合抗血管生成靶向药物(如多纳非尼联合 ICI s[458])、ICIs 联合含奥沙利铂的系统化疗以及双ICIs联合抗血管生成药物和含奥沙利铂的系统化疗(如Ⅱ/Ⅲ期DUBHE-H-308研究[459],Ⅱ期阶段结果显示ORR40%、DCR 90%、mPFS 13.1 个月、12 个月 OS 率 73.3%,Ⅲ期阶段正在进行)等研究,均在一线治疗不可切除的肝癌研究和实践中,已经显示出良好的有效性和安全性。有关的大型临床研究正在进一步积极推进,其结果有望为肝癌一线治疗提供更多的、更好的方案以及充分的循证医学证据,值得期待。
- 二线系统治疗
目前二线治疗药物的适应证获批是基于针对一线索拉非尼或系统化疗失败后与安慰剂对照的Ⅲ期临床研究。对于一线接受免疫联合方案、免疫单药或酪氨酸激酶抑制剂单药治疗的患者,二线治疗方案国内外目前尚未提供高级别循证医学证据。
(1)瑞戈非尼:在多国被批准用于既往接受过索拉非尼治疗的肝癌患者(证据等级 1,推荐 A)。国际多中心Ⅲ期RESORCE 研究[460]评估了瑞戈非尼用于索拉非尼治疗后出现进展的肝癌患者的疗效和安全性。其结果显示,与安慰剂相比,瑞戈非尼组患者死亡风险显著降低 37%,疾病进展风险下降 54%。常见不良反应为高血压、手足皮肤反应、乏力及腹泻等。其不良反应与索拉非尼类似,因此,不适合用于那些对索拉非尼不能耐受的患者。
(2)阿帕替尼:在我国被批准单药用于既往接受过至少一线系统性抗肿瘤治疗后失败或不可耐受的晚期肝癌患者(证据等级 1,推荐 A)。阿帕替尼单药二线治疗中国晚期肝癌的全国多中心Ⅲ期临床研究(AHELP 研究)[461]结果表明,与安慰剂相比,阿帕替尼能够显著延长二线或以上治疗的晚期肝癌患者的 mOS(8.7 个月 vs. 6.8 个月;HR=0.785,95% CI=0.617~0.998,P=0.048)和 mPFS(4.5 个月 vs. 1.9 个月;HR=0.471,95% CI=0.369~0.601,P<0.001)。死亡风险降低 21.5%,疾病进展风险下降 52.9%。同时阿帕替尼组的ORR 达 10.7%,显著高于对照组的 1.5%。常见不良反应是高血压、蛋白尿、白细胞减少症以及血小板减少症等。由于个体差异明显,在使用阿帕替尼过程中,应密切观察随访患者的不良反应,可以根据患者的耐受性给予必要的剂量调整。
(3)雷莫西尤单抗:在多国被批准用于既往接受过索拉非尼治疗且血清 AFP≥400 ng/mL 的肝癌患者的治疗(证据等级 1,推荐 A)。REACH-2 研究[462]结果显示,在既往索拉非尼治疗失败,血清 AFP≥400 ng/mL 的晚期肝癌患者中,与安慰剂相比,雷莫西尤单抗可以显著改善患者的 OS 和 PFS,死亡风险降低 29.0%,疾病进展风险下降 54.8%。REACH-2China 扩展研究[463]结果提示,与安慰剂相比,雷莫西尤单抗显著延长既往接受过索拉非尼治疗且血清 AFP≥400 ng/mL的中国肝癌患者的 mOS(9.1 个月 vs. 6.2 个月,HR=0.854,95% CI=0.536~1.359 ) 和 mPFS ( 2.8 个 月 vs.1.5 个 月 ,HR=0.488,95% CI=0.304~0.785)。死亡风险降低 14.6%,疾病进展风险降低 51.2%。常见不良反应为疲劳、外周水肿、高血压和食欲下降。
(4)帕博利珠单抗:在我国获得批准单药用于治疗既往接受过索拉非尼或含奥沙利铂化疗的肝癌患者(证据等级1,推荐 A)。KEYNOTE-394 亚太区国际多中心研究[464]评估帕博利珠单抗或者安慰剂联合最佳支持治疗对此前接受索拉非尼或奥沙利铂化疗的亚洲晚期肝癌患者的疗效,其中80%的患者来自中国。结果显示,帕博利珠单抗组与安慰剂相比,显著改善患者的 mOS(14.6 个月 vs. 13.0 个月,HR=0.79,95% CI=0.63~0.99,P=0.0180)和 mPFS(2.6 个月vs.2.3 个月,HR=0.74,95% CI=0.60~0.92,P=0.0032)。死亡风险降低 21%,疾病进展风险降低 26%。帕博利珠单抗组的 ORR 为 12.7%,显著高于安慰剂组 1.3%(95% CI=0.2~4.6,P<0.0001)。常见的不良反应为 AST/ALT 升高、皮疹、瘙痒和血胆红素升高。
(5)卡瑞利珠单抗:在我国获得批准用于既往接受过索拉非尼治疗和(或)仑伐替尼治疗和(或)含奥沙利铂系统化疗的晚期肝癌患者的治疗(证据等级 3,推荐 B)。卡瑞利珠单抗在既往系统抗肿瘤治疗过的中国肝癌的Ⅱ期临床研究[465]结果显示,ORR 为 14.7%,6 个月 OS 率为 74.4%,12 个月 OS 率为 55.9%。常见的不良反应是 RCCEP、AST升高、ALT 升高、甲状腺功能减退和乏力等。多项临床研究[466-467]表明,卡瑞利珠单抗与阿帕替尼联合应用后,RCCEP的发生率明显降低。
(6)替雷利珠单抗:在我国获得批准用于既往接受过索拉非尼或仑伐替尼或含奥沙利铂全身化疗的晚期肝癌患者的治疗(证据等级 3,推荐 B)。一项国际多中心的Ⅱ期研究(RATIONALE-208)[468],旨在评估替雷利珠单抗用于治疗既往接受过至少 1 种全身治疗的不可切除肝癌的疗效和安全性的结果显示,mPFS 2.7 个月,mOS 达到 13.2 个月,且总人群的 ORR 为 13%。替雷利珠单抗单用的安全性良好,主要不良反应为 AST 升高、ALT 升高、无力、瘙痒和甲状腺功能减退等。
(7)其他二线系统治疗:美国 FDA 曾经批准纳武利尤单抗联合伊匹木单抗用于既往索拉非尼治疗后进展或无法耐受索拉非尼的肝癌患者[469],卡博替尼用于索拉非尼一线治疗后失败进展的肝癌患者[470],但是在我国没有申请和获得批准。ICIs 治疗与靶向药物、化疗药物、局部治疗等的联合方案 , 以 及 双 靶 点 ICIs ( PD-1/CTLA-4 双 特 异 性 抗 体 、PD-1/VEGF 双特异性抗体等)用于肝癌的二线治疗的研究,都在探索之中。
- 系统抗肿瘤治疗的选择
鉴于目前ICIs为主的治疗已经成为肝癌一线治疗的优先推荐。临床上在选择系统治疗时,应该在充分尊重患者治疗意愿,全面评估患者的体质状况、基础疾病、肿瘤负荷、病理分型、肝功能储备及器官功能状态的基础上,同时,综合考虑治疗目标、药物的作用机制、安全性、耐受性、可及性以及医保政策覆盖等情况,在遵循指南的基础上,制定个体化的治疗方案。
如前所述,至于一线接受过含 ICIs 方案治疗的失败进展患者,现有的已经获批的二线治疗药物均缺乏可以用于治疗的高级别循证医学证据,目前可以根据疾病进展情况及一线治疗的具体方案,可以考虑选择试用未曾使用过的一线治疗药物或已经获批的二线治疗药物,建议在知情同意的前提下,自愿参加新的临床研究。
irAEs 主要是由于免疫系统过度激活,常累及皮肤、结肠、内分泌器官、肝脏及肺等多个部位。其严重程度多数为1~2 级(轻度至中度),但少数情况下可出现严重反应,甚至危及生命。为降低相关风险,免疫治疗前需对患者肿瘤情况及基础器官功能进行充分基线评估,明确 irAEs 发生易感性。基线检查应涵盖病史询问、体格检查、影像学检查、血液学检查,以及甲状腺、垂体、肾上腺功能检查等核心项目。治疗全程及治疗结束后,均应密切监测患者的临床表现(症状与体征)、实验室检查指标、脏器功能以及医学影像学变化,全面评估,警惕 irAEs 发生,包括治疗结束后延迟出现的毒性反应。停药指征:≥3 级不良事件暂停治疗,≥4 级或不可逆毒性终止治疗。具体管理方案,建议参考《中国临床肿瘤学会(CSCO)免疫检查点抑制剂相关的毒性管理指南》和《NCCN 免疫检查点抑制剂相关毒性管理临床实践指南》等。
贝伐珠单抗具有引起出血的风险,建议使用贝伐珠单抗或贝伐珠单抗类似物治疗前,接受胃镜检查,评估高危静脉曲张或其他胃肠道出血风险,并且依据相关指南进行治疗和密切观察。对于最近 6 个月内发生过胃肠道出血和内镜检查显示高危出血风险的患者,慎用贝伐珠单抗或贝伐珠单抗类似物,治疗前必须充分治疗食管胃底静脉曲张,或选用其他治疗方案。
系统抗肿瘤治疗对于中重度肝功能不全患者(肝功能Child-Pugh 评分 7 分以上)的研究数据有限,此类患者需在主诊医师指导下谨慎使用,严密观察,动态监测肝肾功能等,积极防治不良反应。
- 抗肿瘤系统治疗的疗效评价
对于接受抗肿瘤系统治疗的患者,建议在治疗开始的前6 个月内,除了观察临床表现,每 6~8 周复查血清肿瘤标志物和医学影像学;后续可结合血清肿瘤标志物的检测,每9~12 周进行 1 次医学影像学复查,全面评估。目前,对于疗效评价,临床研究和实践中大多数都采用 RECIST 1.1 标准进行;采用抗血管靶向治疗的患者,可以参考 mRECIST 标准;至于接受 ICIs 治疗的患者,还可结合应用 iRECIST 标准[471]。
- 中医药治疗
在辨病论治[472]和中西医结合临床医学体系指导下,针对肝癌早期、中晚期、终末期等不同阶段,采取病证结合[473]临床诊疗的模式,以肝癌的核心病机“癌毒盛衰”为着眼点,综合运用中医方药、现代中药制剂以及中医药特色诊疗技术,与现代医学技术互补协作,形成系统规范方案,以期达到协同抗癌、提高治疗耐受性、减少术后并发症、预防复发转移、减轻不良反应及延长生存期的作用。
(1)中医方药分阶段治疗
中医治疗肝癌强调分期论治、辨证施治。根据肿瘤分期及患者整体状况的不同,可将治疗过程分为早期、中晚期及终末期三个阶段,各阶段治疗目标和证候特点有所差异。
在早期肝癌(CNLC Ⅰa~Ⅰb 期),治疗重点在于围手术期的整体调理。术前应重视辨证论治,以维护肝功能、增强机体免疫力、提高手术成功率并减少术后并发症;术后则多从正气受损、癌毒未净的角度出发,着重预防肿瘤复发和转移。此阶段常见的证候包括肝气郁结证和气滞血瘀证。肝气郁结证多表现为胁肋胀满或胀痛、脘腹痞满、胸闷、善太息、情志抑郁或急躁易怒,舌质淡红、苔薄白、脉弦,治疗以疏肝理气解郁为法,常选用《景岳全书》柴胡疏肝散加减,方中可用柴胡、陈皮、白芍、枳壳、香附、川芎、郁金、八月札、石见穿、土茯苓、鸡内金及甘草等,常规剂量,每日 2次水煎服。气滞血瘀证则多见上腹肿块、胁肋刺痛且痛有定处,或夜间疼痛加重,并可伴有肝掌、蜘蛛痣、腹壁青筋暴露,舌边瘀暗或暗红,脉弦细或细涩无力,治疗宜活血化瘀、软坚散结,常选用《医林改错》膈下逐瘀汤加减,如生地、当归、赤芍、川芎、桃仁、红花、五灵脂、枳壳、桔梗、甘草、柴胡、玄参等,常规剂量,每日 2 次水煎服。
在中晚期肝癌(CNLC Ⅱa~Ⅲb 期),治疗应以控制癌毒、延缓肿瘤进展为核心,强调现代医学治疗手段与中医药扶正抗癌的结合,以减少或缓解并发症、提高疗效并改善生活质量。常见证候包括肝郁脾虚证和湿热毒蕴证。肝郁脾虚证多表现为胸腹胀满、食后加重、倦怠乏力、消瘦纳差、大便溏薄,严重者可见腹水、黄疸及下肢水肿,舌质胖大、苔白、脉濡缓兼弦,治疗宜疏肝健脾、理气消癥,可选用《太平惠民和剂局方》逍遥散加减,如柴胡、当归、白芍、党参、白术、茯苓、薏苡仁、半枝莲、七叶一枝花、干蟾皮、蜈蚣、厚朴及甘草等。湿热毒蕴证多见胁肋胀痛拒按、发热、口苦口臭、身目发黄、小便短赤、大便秘结或黏腻不爽,舌质红、苔黄腻、脉滑数,治疗以清热利湿、解毒消癥为法,常选用《伤寒论》茵陈蒿汤合五苓散加减,可用茵陈蒿、大黄、栀子、猪苓、茯苓、白术、泽泻,并配伍虎杖、白花蛇舌草、八月札、半枝莲、赤芍、人工牛黄、猫人参、石见穿、山慈菇、鸡内金等。
在终末期肝癌(CNLC Ⅳ期),多属癌毒炽盛、正气亏虚之候,治疗应以扶正为主,强调整体调节,旨在减轻症状、改善生活质量并适当延长生存期。此阶段常见肝肾不足、气阴两亏等证候,临床表现为消瘦乏力、短气喘促、颧红口干、潮热或手足心热、寐浅易醒,甚或出现齿衄、鼻衄及二便下血,舌红少苔、脉细数无力。治疗宜益气养阴、扶正消癥,常选用《柳州医话》一贯煎加减,可用生地黄、麦冬、沙参、枸杞子、五味子、黄芪、当归、党参、白术、茯苓、山茱萸、西洋参,并配伍八月札、龟板、鳖甲、猫人参、石见穿、山慈菇、鸡内金等,常规剂量,每日 2 次水煎服。
(2)现代中药制剂治疗
阿可拉定(淫羊藿素)软胶囊是一种从天然药用植物暨传统草本中药淫羊藿中提取、分离和纯化获得的单分子创新药物,具有抑制肿瘤生长、调节免疫等多重作用[474]。在我国已经附条件批准用于不适合标准治疗的晚期肝癌患者的治疗,具体的适应证:不适合或拒绝接受标准治疗,且既往未接受过全身系统性治疗的、不可切除的肝癌患者,同时患者外周血复合标志物满足以下检测指标的至少 2 项:AFP≥400ng/mL;TNF-ɑ <2.5 pg/mL;IFN-γ≥7.0 pg/mL。
除阿可拉定软胶囊外,我国国家药品监督管理局已经批准了若干种现代中药制剂用于治疗晚期肝癌,包括槐耳颗粒、华蟾素制剂、通关藤制剂、榄香烯注射液、康莱特注射液、康艾注射液、肝复乐胶囊、金龙胶囊和慈丹胶囊等[475-481]。另外,槐耳颗粒可以用于肝癌手术切除后的辅助治疗[232]。
(3)中医药特色诊疗技术
①针灸治疗:根据病情及临床实际可以选择应用体针、头针、电针、耳针、腕踝针、眼针、灸法、穴位埋线、穴位敷贴、耳穴压豆和拔罐等方法。针灸治疗的取穴以肝俞、足三里为主穴,配以阳陵泉、期门、章门、三阴交等;穴位敷贴以章门、期门、肝俞、内关、公孙主穴,疼痛者配外关、足三里、阳陵泉;腹水配气海、三阴交、阴陵泉等。②其他治疗:根据病情酌情使用活血化瘀、清热解毒等中药、中成药,进行外敷治疗、中药泡洗、中药熏洗等。
- 抗病毒治疗
所有确诊为肝癌的患者,必须常规检查肝炎病毒,包括HBV 和 HCV 感染的标志物,主要是乙型肝炎“两对半”,包括 HBsAg、HBsAb、HBeAg、HBeAb、HBcAb 等五项指标;HBsAg 阳性或 HBcAb 阳性患者,则应进一步定量检测血清HBV DNA。
HBV 相关肝癌患者,只要是 HBsAg 阳性,无论是否可以检测出 HBV DNA,均应立即启动抗病毒治疗[482]。对于HBV 相关肝癌患者,推荐及时使用高耐药屏障的核苷(酸)类抗病毒药物,包括恩替卡韦、替诺福韦酯、丙酚替诺福韦、艾米替诺福韦或者普雷福韦[482-483](证据等级 1,推荐 A)。准备进行肝移植的 HBV 感染者,如果 HBsAg 阳性,建议在肝移植前开始应用上述药物进行抗 HBV 治疗(证据等级 1,推荐 A)。即使是 HBsAg 阴性患者,如果接受 HBsAg 阳性或HBsAg 阴性但抗-HBc 阳性的移植物时,也应当接受长期、规范化的抗 HBV 治疗,以预防 HBV 再激活和造成感染。
合并 HBV 感染的肝癌患者,口服核苷(酸)类似物抗病毒治疗时,应该注意需要贯穿于整个治疗的全过程。无论接受核苷(酸)类似物抗病毒治疗与否,都应密切监测,每3~6 个月复查乙型肝炎“两对半”、HBV DNA 和肝肾功能等指标。推荐优先采用高灵敏血清 HBV DNA 检测,以便及时识别低病毒血症患者。HBsAg 阳性者需长期抗病毒,且不依赖HBV DNA,对于已经接受抗病毒治疗但是有低病毒血症的患者,需要进一步处理,通常要调整治疗策略,可以选择更换更加强效低耐药的一线核苷(酸)类似物(NAs),或在评估患者耐受情况后联合其他抗病毒药物,要将 HBV DNA 降至高灵敏检测的检出下限以下,实现持续病毒抑制,以降低进展、复发等风险。
对于 HCV 相关肝癌,HCV 抗体或 HCV RNA 阳性者,建议采用 DAAs 进行抗病毒治疗(证据等级 1,推荐 A)。抗病毒治疗终点为治疗结束后 12 周,采用敏感检测方法检测不到血清或血浆中 HCV RNA。目前,DAAs 可使 95%以上的 HCV 感染者实现病毒治愈[484]。
- 保肝、利胆及对症支持治疗
肝癌患者在自然病程中或治疗过程中可能会伴随肝功能碍,包括肝酶和(或)胆红素异常增高,应及时而适当地使用保肝、利胆、抗氧化和解毒的药物,包括联苯双酯、双环醇、异甘草酸镁注射液、甘草酸二铵、复方甘草酸苷、多烯磷脂酰胆碱、水飞蓟素、还原型谷胱甘肽、乌司他丁、腺苷蛋氨酸、熊去氧胆酸、消炎利胆片以及苦黄注射液等。肝癌患者往往合并有肝硬化、门静脉高压、脾脏肿大和脾功能亢进,并且可能由于抗肿瘤治疗而导致一系或多系的血细胞减少,应考虑给予药物治疗或血制品输注。比如,对于白细胞和(或)中性粒细胞减少患者,可酌情给予粒细胞集落刺激因子(G-CSF,包括 PEG-rhG-CSF 和 rhG-CSF)[485]。血红蛋白<80 g/L 的患者,可根据贫血的病因和分类,给予铁剂、叶酸、维生素 B12 和促红细胞生成素(EPO)等治疗。由于慢性肝病引起血小板减少的患者,根据病情需要可以使用重组人血小板生成素(rh-TPO)或血小板生成素受体激动剂(TPO-RA,如海曲泊帕、阿伐曲泊帕及芦曲泊帕)等药物[486-487],促进血小板生成。
在肝癌治疗的全程,特别是终末期肝癌患者,应该积极给予最佳支持治疗和防治并发症治疗,包括加强营养支持,镇痛、纠正低白蛋白血症、控制合并糖尿病患者的血糖水平,及时控制腹腔积液、处理黄疸、肝性脑病、消化道出血及肝肾综合征等并发症。针对有症状的骨转移患者,可以酌情使用双膦酸盐类药物(氯膦酸钠、伊班膦酸钠和唑来膦酸等)或地舒单抗。需要注意长期使用强效的第三代双膦酸盐药物(伊班膦酸钠和唑来膦酸等)可能导致颌骨坏死、食管癌和肾功能衰竭等严重不良反应,应关注其安全性问题,警惕相关风险。另外,适度的康复运动可以增强患者的免疫功能。同时,还要重视患者的心理干预,增强患者战胜疾病的信心,把消极心理转化为积极心理,通过合理的舒缓疗护,使患者享有安全感、舒适感,从而减少抑郁与焦虑,改善生存质量。
要点论述:
(1)系统抗肿瘤治疗在不可手术切除的中晚期肝癌中的适应证主要为:CNLC Ⅲa、Ⅲb 期肝癌患者,不适合手术切除或 TACE 治疗的 CNLC Ⅱb 期肝癌患者;TACE 治疗抵抗或 TACE 治疗失败的肝癌患者;可以与经动脉介入治疗联合,治疗 CNLC 分期Ⅱb、Ⅲa、Ⅲb 期的肝癌。
(2)一线系统抗肿瘤治疗方案可以优先选择阿替利珠单抗联合贝伐珠单抗、纳武利尤单抗联合伊匹木单抗、阿帕替尼联合卡瑞利珠单抗、信迪利单抗联合贝伐珠单抗类似物、菲诺利单抗联合贝伐珠单抗、特瑞普利单抗联合贝伐珠单抗或者安罗替尼联合派安普利单抗。多纳非尼、仑伐替尼、替雷利珠单抗、索拉非尼或者 FOLFOX4 方案的系统化疗仍然可用于肝癌的一线治疗。
(3)二线系统抗肿瘤治疗方案,在我国可以选择瑞戈非尼、阿帕替尼、帕博利珠单抗、雷莫西尤单抗(血清AFP≥400 μg/L)、卡瑞利珠单抗或替雷利珠单抗。对于一线接受免疫联合方案、免疫单药或酪氨酸激酶抑制剂单药治疗的患者,二线治疗方案选择可以考虑根据疾病进展方式和具体一线方案不同,选择未曾使用过的一线治疗的药物或获批的二线治疗药物,鼓励患者自愿参加新药的临床试验。
(4)可根据病情选择传统中医药治疗。除了阿可拉定软胶囊外,我国已经批准了若干种现代中药制剂用于治疗晚期肝癌。另外,槐耳颗粒可以用于肝癌手术切除后的辅助治疗。
(5)在抗肿瘤治疗的同时,抗病毒治疗应始终贯穿治疗全过程。对于 HBV 相关肝癌患者,推荐及时使用高耐药屏障的核苷(酸)类抗病毒药物,包括恩替卡韦、替诺福韦酯、丙酚替诺福韦、艾米替诺福韦或者普雷福韦。
(六)肝癌自发破裂的治疗
肝癌自发破裂是肝癌潜在的致死性并发症,单纯保守治疗在院病死率极高,但并非影响患者长期生存的决定因素,获得手术切除可以使部分患者具有明显的生存获益。因此,在最初抢救成功后,应充分评估患者血流动力学、肝功能、全身情况、肿瘤初始分期及可切除性进行个体化决策,推荐采用 MDT 模式制定治疗方案[488-492]。对于肝肿瘤可切除、肝脏储备功能良好、血流动力学稳定的患者,急诊肝切除术,可以提供显著的生存获益[493-497](证据等级 3,推荐 B)。对于肝肿瘤不可切除或肝脏储备功能差的患者,可以选择TAE/TACE 止血,后续与靶向药物和(或)ICIs 相结合有助于改善部分患者的预后[498-500](证据等级 4,推荐 B)。肝癌自发破裂是手术后的高危复发因素,术中应充分地冲洗腹腔;术后辅助治疗有助于延长生存[501-502];术后应加强监测,术后单纯腹膜转移的患者可以考虑行积极根治性切除[503](证据等级 3,推荐 C)。
要点论述:
(1)肝癌自发破裂是肝癌潜在的致死性并发症,应充分评估患者血流动力学、肝功能、全身情况、肿瘤初始分期及可切除性进行个体化决策,推荐采用 MDT 模式制定治疗方案,介入和(或)靶向/免疫治疗可能改善部分患者的预后,但需平衡疗效与安全性。
六、声明
指南的编撰工作独立于任何赞助单位,并且所有编写人员都承诺过编撰内容与是否受到资助无关。



- 肝癌高风险人群监测方案及简化序列 MRI
研究发现在肝硬化患者中,使用肝胆特异性对比剂 MRI监测方案检出超早期肝癌的敏感度可达到 72.1%[504]。使用常规对比剂 MRI 检出直径 1~2 cm 肝癌的敏感性仍高于超声造影检查[505]。简化序列磁共振成像(abbreviated MRI,aMRI),许时,可使用 MRI+AFP 的监测方案对肝癌超高风险人群进行 6 个月 1 次的监测,以提高早期肝癌检出率。如使用动态增强 MRI 进行监测,扫描序列可参考附录 4;如使用 aMRI进行监测,建议扫描序列为:抑脂轴位-T2WI;轴位 DWI;轴位 T1WI 正反相位;轴位抑脂 3D-T1WI-GRE(所有序列均为屏气序列且层厚≤3 mm),以防漏诊亚厘米肝癌。
肝癌的液体活检
液体活检技术具有无创取样、多次检测、高度敏感等特性,常用标志物包括循环肿瘤细胞(circulating tumor cell,CTC)、循环游离 DNA(cell-free DNA,cfDNA),循环肿瘤DNA(circulating tumor DNA,ctDNA)等,在肝癌的早期筛查及诊断、预后评估、疾病监测、疗效评估中展现出较高价值[508]。
CTC 检测可以成为一种肝癌预后预测和疗效评价的临床新工具[96,509]。有报道,外周血 EpCAM+ CTC 具有干细胞样特性,是肝癌切除术后早期复发转移的独立预测指标[510];检测 CTC 总体负荷、CTC 异质性亚型对肝癌患者 TACE 治疗后及放射治疗后肿瘤复发转移和进展具有预测作用[511-512];不同部位、不同时点检出的 CTC 能预测不同器官转移类型[513-514];术前 CTC 负荷可以指导外科手术切缘大小,降低复发转移可能[515]。此外,动态检测 CTC 可以用于监控肝癌肝移植术后肿瘤复发转移[516]。
cfDNA 是通过细胞凋亡、坏死和分泌释放到血液中的DNA 物质。在癌症患者中,总 cfDNA 的主要成分是由肿瘤细胞释放的特异性突变 DNA 片段,即 ctDNA 组成,能够反映肿瘤的遗传信息。据报道,ctDNA 用于肝癌早期诊断的敏感性和特异性均优于血清 AFP [98,517],还可以动态反映肝癌手术切除效果[518-519]、评估仑伐替尼、ICIs 治疗的疗效[128,520]。有研究报道利用外周血低覆盖率全基因组 cfDNA 片段组学特征,可实现肝癌早诊和鉴别诊断,曲线下面积(AUC)达0.995,有望在临床推广应用[97]。
近期研究发现,利用特定基因表观遗传修饰特征,如甲基化[521],5-hmc [99,522]等也可以用于肝癌早期诊断。基于外周血 cfDNA 甲基化检测的 ELSA-seq 技术平台,所建立的MCDBT-1 模型可以用于癌症溯源和肝癌早筛,显著优于其他癌种[523]。也有研究报道,通过对 cfDNA 的体细胞突变和甲基化特征的多重同步分析,相互补充,可以更为有效地发现早期肝癌[524]。
此外,其他新型液体活检标志物如血清自身抗体[525]、血浆代谢物[526]、肿瘤相关血小板(tumor-educated platelets,TEPs)[527]、循环 T 细胞受体库(T-cell receptors,TCR)[528]、外周血免疫细胞亚群检测[529]等在肝癌早期诊断、疗效监测中也表现出一定潜力。
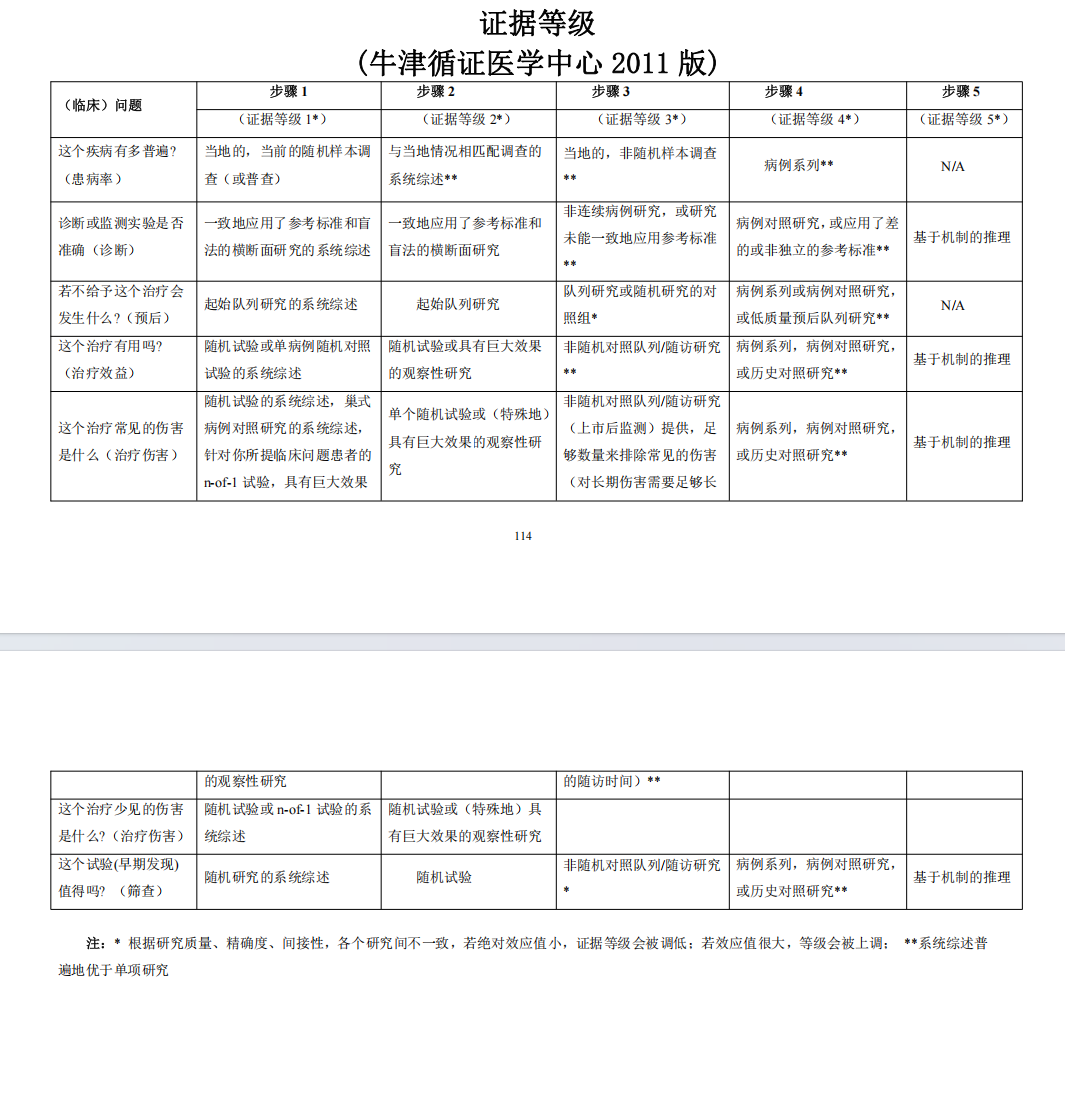
肝癌的大体分型
参照中国肝癌病理研究协作组大体病理分型,并与中国肝癌临床分期相对应,在巨检描述时可将肝癌分为五型:
(1)弥漫型:弥漫性肿瘤小结节全肝分布;
(2)巨块型:最大直径肿瘤≥10 cm 的单发或多发肿瘤;
(3)块状型:最大直径肿瘤介于 5~10 cm 的单发或多发肿瘤;
(4)结节型:最大直径肿瘤≤5 cm 的单发或多发肿瘤;
(5)小癌型:特指结节型 HCC 中,单个肿瘤且肿瘤直径≤3 cm,是 HCC 生物学行为演进的重要节点

肝癌外放射治疗正常组织
具体耐受剂量参考
- 立体定向放射治疗
(1)肝功能 Child-Pugh A 级,放射治疗分次数 3~5 Fx,正常肝体积[肝脏体积-大体肿瘤体积,Liver-Gross tumorvolume(GTV)]>700 mL 或>800 mL,Liver-GTV 平均剂量分别<15 Gy 或<18 Gy;放射治疗分次数 6 Fx,Liver-GTV 体积>800 mL,平均剂量<20 Gy;每次肿瘤分割剂量 4~8 Gy,Liver-GTV 平均剂量<23 Gy 为安全剂量[530-531](证据等级 3,推荐 B)。
(2)亚洲肝癌患者常伴有肝硬化和脾功能亢进,导致胃肠道瘀血和凝血功能差,胃肠道的放射耐受剂量低于RTOG 推荐的剂量[532];目前文献及专家共识认为,放射治疗分次数 3~5 Fx,胃和小肠最大剂量均应<22.2~35 Gy,最佳<30 Gy。
(3)放射治疗分次数 3~5 Fx,双肾平均剂量最佳<10Gy,脊髓最大剂量<21.9~30 Gy,最佳<18~23 Gy [533]。
- 常规分割剂量放射治疗
(1)肝功能 Child-Pugh A 级患者,Liver-GTV 平均剂量<28~30 Gy;肝功能 Child-Pugh B 级患者,肝脏对射线的耐126受量明显下降,最佳<6 Gy,避免肝功能 Child-Pugh C 级患者行肝区放射治疗[531]。
(2)胃和小肠最大剂量均应<54 Gy,胃 V45<45%,小肠 V50≤5%。
(3)双肾平均剂量≤15 Gy,如一侧肾脏平均剂量>19Gy,则另一侧肾脏尽量避开;脊髓最大剂量<45 Gy [530]。















